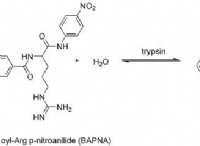
Που επηρεάζει το σχήμα του μορίου;
1. Ο αριθμός των ζευγών ηλεκτρονίων γύρω από το κεντρικό άτομο: Αυτό διέπεται από τη θεωρία του ζεύγους Electron (VSEPR) . Τα ζεύγη ηλεκτρονίων (τόσο ζεύγη συγκόλλησης όσο και μοναχικά ζεύγη) γύρω από το κεντρικό άτομο θα οργανώσουν τον εαυτό τους για να ελαχιστοποιήσουν την απόρριψη, οδηγώντας σε συγκεκριμένα γεωμετρικά σχήματα.
2. Ο τύπος των ομολόγων (μονή, διπλή ή τριπλή): Οι διπλοί και τριπλοί δεσμοί καταλαμβάνουν περισσότερο χώρο από τους μεμονωμένους δεσμούς, οι οποίοι μπορούν να επηρεάσουν τις γωνίες των δεσμών και το συνολικό σχήμα.
3. Η παρουσία μοναχικών ζευγών στο κεντρικό άτομο: Τα ζεύγη Lone είναι πιο απωθητικά από τα ζεύγη συγκόλλησης, προκαλώντας τους να ωθήσουν τα ζεύγη συγκόλλησης πιο κοντά και να παραμορφώσουν το σχήμα του μορίου.
4. Υβριδισμός τροχιακών: Η ανάμειξη ατομικών τροχιακών σε υβριδικά τροχιακά επηρεάζει τη γεωμετρία του μορίου. Για παράδειγμα, ο υβριδισμός SP3 οδηγεί σε τετραεδρικό σχήμα, ενώ ο υβριδισμός SP2 έχει ως αποτέλεσμα ένα τριγωνικό επίπεδο.
5. Διαμοριακές δυνάμεις: Αν και δεν καθορίζουν άμεσα το σχήμα του μορίου, οι διαμοριακές δυνάμεις όπως η δέσμευση υδρογόνου μπορούν να επηρεάσουν τη συνολική διάταξη των μορίων σε υγρή ή στερεά κατάσταση.
Συνοπτικά, το σχήμα ενός μορίου είναι συνέπεια της ισορροπίας μεταξύ της απόρριψης των ζεύγους ηλεκτρονίων, της επίδρασης των τύπων δεσμών και της παρουσίας μοναχικών ζευγών, όλα μέσα στο πλαίσιο της ατομικής τροχιακής υβριδοποίησης.