Διαφορά μεταξύ θρυψίνης και χυμοθρυψίνης
Η κύρια διαφορά μεταξύ θρυψίνης και χυμοθρυψίνης είναι ότι το t Η ρυψίνη διασπά στα καρβοξυτελικά υπολείμματα αργινίνης και λυσίνης ενώ η χυμοθρυψίνη διασπά στα καρβοξυτελικά υπολείμματα φαινυλαλανίνης, τρυπτοφάνης και τυροσίνης. Αυτό σημαίνει ότι η τρυψίνη δρα στα βασικά αμινοξέα ενώ η χυμοθρυψίνη δρα στα αρωματικά αμινοξέα.
Η θρυψίνη και η χυμοθρυψίνη είναι δύο τύποι πρωτεϊνικών πεπτικών ενζύμων που διασπούν τους πεπτιδικούς δεσμούς στο καρβοξυτελικό άκρο. Εκκρίνονται από τους εξωκρινείς αδένες του παγκρέατος στις ανενεργές τους μορφές που ονομάζονται ζυμογόνα.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η τρυψίνη
– Ορισμός, Γεγονότα, Ρόλος
2. Τι είναι η Χυμοθρυψίνη
– Ορισμός, Γεγονότα, Ρόλος
3. Ποιες είναι οι ομοιότητες μεταξύ της θρυψίνης και της χυμοθρυψίνης
– Περίληψη κοινών χαρακτηριστικών
4. Ποια είναι η διαφορά μεταξύ θρυψίνης και χυμοθρυψίνης
– Σύγκριση βασικών διαφορών
Βασικοί όροι
Χυμοθρυψίνη, Χυμοθρυψινογόνο, Πάγκρεας, Πρωτεολυτικά Ένζυμα, Τρυψίνη, Τρυψινογόνο
Τι είναι η τρυψίνη
Η θρυψίνη είναι μια πρωτεάση σερίνης με ειδικότητα υποστρώματος προς τα βασικά αμινοξέα όπως η λυσίνη και η αργινίνη. Παράγεται από το πάγκρεας και εκκρίνεται στην ανενεργή του μορφή που ονομάζεται τρυψινογόνο. Η ενεργοποίηση του τρυψινογόνου γίνεται με την απομάκρυνση του τερματικού εξαπεπτιδίου με τη δράση της εντεροκινάσης. Οι δύο κύριοι τύποι θρυψίνης είναι η α- και η β-θρυψίνη.
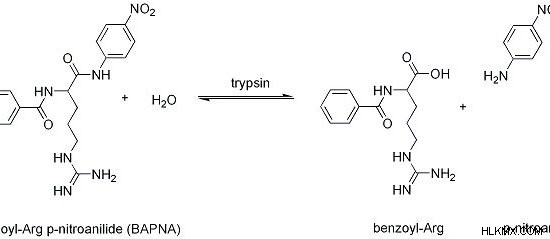
Εικόνα 1:Μηχανισμός δράσης θρυψίνης
Η θρυψίνη είναι ένα σημαντικό ένζυμο που χρησιμοποιείται για άλλους σκοπούς εκτός από τη λειτουργία του στο πεπτικό σύστημα. Χρησιμοποιείται επίσης στη διάσταση ιστού και στη συλλογή κυττάρων από καλλιέργειες.
Τι είναι η χυμοτρυψίνη
Η χυμοτρυψίνη είναι μια ενδοπεπτιδάση σερίνης με ειδικότητα υποστρώματος προς τις πλευρικές αλυσίδες φαινυλαλανίνης, τρυπτοφάνης και τυροσίνης, οι οποίες είναι κυρίως μεγάλα υδρόφοβα υπολείμματα. Παράγεται από κυλινδρικά κύτταρα του παγκρέατος και εκκρίνεται στην ανενεργή του μορφή που ονομάζεται χυμοθρυψινογόνο. Η ενεργοποίηση του χυμοθρυψινογόνου γίνεται βασικά από την ενζυματική δράση της θρυψίνης. Οι δύο κύριοι τύποι χυμοθρυψίνης είναι η χυμοθρυψίνη Α και Β.
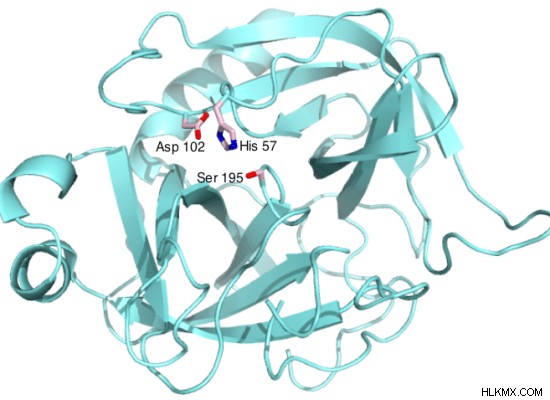
Εικόνα 2:Ενεργό σημείο χυμοθρυψίνης
Η δομή της θρυψίνης και της χυμοθρυψίνης είναι παρόμοια εκτός από τη θέση S1 της χυμοθρυψίνης, η οποία δίνει την ειδική για το υπόστρωμα κατάλυση της χυμοθρυψίνης.
Similarities Between Trypsin and Chymotrypsin">Similarities Between Trypsin and Chymotrypsin
- Η θρυψίνη και η χυμοθρυψίνη είναι πρωτεολυτικά ένζυμα που εκκρίνονται από το πάγκρεας.
- Απελευθερώνονται στο λεπτό έντερο στο δωδεκαδάκτυλο.
- Και τα δύο εκκρίνονται στην ανενεργή τους μορφή. Τα υπολείμματα της ενεργού θέσης τόσο της τρυψίνης όσο και της χυμοθρυψίνης είναι η ιστιδίνη, το ασπαρτικό και η σερίνη.
- Βοηθούν στην ενζυματική πέψη των πρωτεϊνών.
- Οι χαμηλές ποσότητες θρυψίνης και χυμοθρυψίνης στα κόπρανα είναι δείκτες κυστικής ίνωσης και παγκρεατικής νόσου, όπως η παγκρεατίτιδα.
Διαφορά μεταξύ θρυψίνης και χυμοθρυψίνης
Ορισμός
Η θρυψίνη αναφέρεται σε ένα πεπτικό ένζυμο που διασπά πρωτεΐνες στο λεπτό έντερο, που εκκρίνεται από το πάγκρεας ως τρυψινογόνο, ενώ η χυμοθρυψίνη αναφέρεται σε ένα πεπτικό ένζυμο που εκκρίνεται από το πάγκρεας και μετατρέπεται σε ενεργό μορφή από τρυψίνη.
Τύποι
Η α- και η β-τρυψίνη είναι οι δύο τύποι θρυψίνης ενώ η χυμοθρυψίνη Α και Β είναι οι δύο τύποι χυμοθρυψίνης.
Ανενεργή φόρμα
Επίσης, η ανενεργή μορφή της θρυψίνης είναι η τρυψινογόνο, ενώ η ανενεργή μορφή της χυμοθρυψίνης είναι χυμοθρυψινογόνο.
Ενεργοποίηση
Επιπλέον, το τρυψινογόνο ενεργοποιείται από την εντεροκινάση ενώ το χυμοθρυψινογόνο ενεργοποιείται από τη θρυψίνη.
Ενζυματική δράση
Επιπλέον, η θρυψίνη υδρολύει τους πεπτιδικούς δεσμούς στην καρβοξυτελική πλευρά της λυσίνης ή της αργινίνης ενώ η χυμοθρυψίνη υδρολύει τους πεπτιδικούς δεσμούς στην C-τερματική πλευρά της φαινυλαλανίνης, της τρυπτοφάνης και της τυροσίνης. Αυτή είναι μια κύρια διαφορά μεταξύ της θρυψίνης και της χυμοθρυψίνης.
Αναστολείς
Επιπλέον, οι αναστολείς της θρυψίνης είναι το DFP, η απροτινίνη, το Ag+, το EDTA, η βενζαμιδίνη κ.λπ., ενώ οι αναστολείς της χυμοθρυψίνης είναι υδροξυμεθυλοπυρρόλες, βορονικά οξέα, παράγωγα κουρμαρίνης δεϋλικά, πεπτίδια , κ.λπ.
Εφαρμογές
Λαμβάνοντας υπόψη τις εφαρμογές, η θρυψίνη χρησιμοποιείται σε διαχωρισμό ιστού, συλλογή κυττάρων, μιτοχονδριακή απομόνωση, in vitro πρωτεϊνικές μελέτες, κ.λπ. ενώ η χυμοθρυψίνη χρησιμοποιείται σε ανάλυση αλληλουχίας, σύνθεση πεπτιδίων, χαρτογράφηση πεπτιδίων , δακτυλικά αποτυπώματα πεπτιδίων, κ.λπ.
Συμπέρασμα
Η θρυψίνη είναι το πεπτικό ένζυμο πρωτεΐνης που διασπά τους πεπτιδικούς δεσμούς στα C-τερματικά βασικά αμινοξέα όπως η λυσίνη και η αργινίνη. Ωστόσο, η χυμοθρυψίνη είναι ένα άλλο πεπτικό ένζυμο πρωτεΐνης που διασπά τους πεπτιδικούς δεσμούς στα C-τερματικά μεγάλα υδρόφοβα αμινοξέα όπως η φαινυλαλανίνη, η τρυπτοφάνη και η τυροσίνη. Τόσο η θρυψίνη όσο και η χυμοθρυψίνη εκκρίνονται από το πάγκρεας στην ανενεργή τους μορφή. Η κύρια διαφορά μεταξύ θρυψίνης και χυμοθρυψίνης είναι ο τύπος της ενζυματικής δράσης.
Αναφορά:
1. «Τρυψίνη». Εγχειρίδιο Catalase – Worthington Enzyme, Διαθέσιμο εδώ
2. «Χυμοθρυψίνη». Catalase – Εγχειρίδιο Worthington Enzyme, Διαθέσιμο εδώ
Εικόνα Ευγενική προσφορά:
1. "BAPNA assay" Από τον Volker Gatterdam – Δικό του έργο (CC BY-SA 3.0) μέσω Commons Wikimedia
2. "Chymotrypsin" By Jcwhizz (CC BY-SA 3.0) μέσω Commons Wikimedia