Τι δείχνει ο αριθμός οξείδωσης;
Εδώ σας λέει:
* κέρδος ηλεκτρονίων ή απώλεια: Ένας θετικός αριθμός οξείδωσης σημαίνει ότι ένα άτομο έχει * χάσει * ηλεκτρόνια, ενώ ένας αρνητικός αριθμός σημαίνει ότι έχει * κερδίσει * ηλεκτρόνια.
* Σχετική ηλεκτροαρνητικότητα: Το άτομο με τον υψηλότερο αριθμό οξείδωσης είναι το πιο ηλεκτροαρνητικό άτομο στον δεσμό.
* Αντιδράσεις οξειδοαναγωγής: Οι αριθμοί οξείδωσης είναι ζωτικής σημασίας για την κατανόηση και την εξισορρόπηση των αντιδράσεων οξειδοαναγωγής, όπου τα ηλεκτρόνια μεταφέρονται μεταξύ των ατόμων.
Βασικά σημεία:
* Είναι μια υποθετική χρέωση: Οι αριθμοί οξείδωσης δεν είναι πραγματικές χρεώσεις. Είναι ένα εργαλείο λογιστικής για την παρακολούθηση της κίνησης των ηλεκτρονίων.
* Εξαρτάται από το μόριο/ιόν: Ο αριθμός οξείδωσης ενός ατόμου μπορεί να αλλάξει ανάλογα με το μόριο ή το ιόν που είναι μέρος του.
* Μπορεί να είναι κλασματική: Οι αριθμοί οξείδωσης μπορούν να είναι κλάσματα, ειδικά σε πολυατομικά ιόντα.
Παράδειγμα:
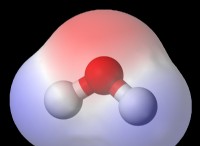
Στο σύνθετο νερό (H₂O), ο αριθμός οξείδωσης του οξυγόνου είναι -2 και ο αριθμός οξείδωσης του υδρογόνου είναι +1. Αυτό σημαίνει ότι το οξυγόνο θεωρείται ότι έχει κερδίσει δύο ηλεκτρόνια (λόγω της υψηλότερης ηλεκτροαρνητικότητάς του) και κάθε άτομο υδρογόνου έχει χάσει ένα ηλεκτρόνιο.
Επιτρέψτε μου να ξέρω αν θέλετε να μάθετε περισσότερα σχετικά με τους αριθμούς οξείδωσης ή συγκεκριμένα παραδείγματα!