Τι είναι γνωστό ως ο διαχωρισμός των ιόντων που συμβαίνουν όταν μια ιοντική ένωση διαλύεται σε ένα διάλυμα;
Εδώ είναι μια κατανομή:
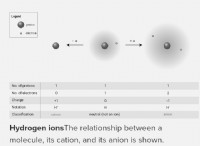
* Ιωνικές ενώσεις: Αυτές οι ενώσεις σχηματίζονται από την ηλεκτροστατική έλξη μεταξύ των αντίθετα φορτισμένων ιόντων.
* Διάλυση: Όταν μια ιοντική ένωση διαλύεται σε έναν διαλύτη (όπως το νερό), τα μόρια του διαλύτη περιβάλλουν τα ιόντα και τα τραβούν χωριστά.
* Διάσπαση: Αυτή η διαδικασία έλξης των ιόντων χωριστά ονομάζεται διάσταση. Τα ιόντα περιβάλλονται από μόρια διαλύτη και τώρα είναι ελεύθερα να κινούνται ανεξάρτητα μέσα στη λύση.
Για παράδειγμα, όταν το χλωριούχο νάτριο (NaCl) διαλύεται στο νερό, συμβαίνει η ακόλουθη διάσταση:
NaCl (s) → Na⁺ (aq) + cl⁻ (aq)
* (s) υποδεικνύει μια στερεά κατάσταση.
* (aq) υποδεικνύει ένα υδατικό διάλυμα (διαλυμένο σε νερό).
Έτσι, το αποτέλεσμα της διάστασης είναι ο σχηματισμός διαλύματος που περιέχει ελεύθερα ιόντα, τα οποία στη συνέχεια μπορούν να διεξάγουν ηλεκτρική ενέργεια.