Ποιο στοιχείο σχηματίζει ιονικό δεσμό;
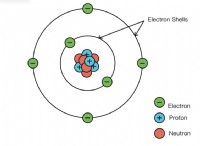
* μέταλλα τείνουν να χάσουν ηλεκτρόνια για να επιτύχουν μια σταθερή διαμόρφωση ηλεκτρονίων (όπως ένα ευγενές αέριο). Αυτό έχει ως αποτέλεσμα να σχηματίζουν θετικά φορτισμένα ιόντα που ονομάζονται κατιόντα .
* Μη μέταλλα τείνουν να κερδίζουν ηλεκτρόνια για να επιτύχουν μια σταθερή διαμόρφωση ηλεκτρονίων. Σχηματίζουν αρνητικά φορτισμένα ιόντα που ονομάζονται anions .
Παράδειγμα:
* νάτριο (na) , ένα μέταλλο, χάνει ένα ηλεκτρόνιο για να γίνει na+ .
* χλώριο (cl) , ένα μη μέταλλο, κερδίζει ένα ηλεκτρόνιο για να γίνει cl- .
Αυτά τα αντίθετα φορτισμένα ιόντα προσελκύουν ο ένας τον άλλον ηλεκτροστατικά, σχηματίζοντας έναν ιονικό δεσμό . Αυτός είναι ο λόγος για τον οποίο το νάτριο και το χλώριο συνδυάζονται για να σχηματίσουν την ιοντική ένωση χλωριούχο νάτριο (NaCl) , επίσης γνωστό ως επιτραπέζιο αλάτι.
Σημαντικές σημειώσεις:
* Δεν είναι όλα τα μέταλλα που σχηματίζουν ιονικούς δεσμούς. Για παράδειγμα, ο υδράργυρος (HG) και ο χρυσός (AU) τείνουν να σχηματίζουν ομοιοπολικούς δεσμούς.
* Ορισμένα μη μέταλλα μπορούν επίσης να σχηματίσουν ομοιοπολικούς δεσμούς. Για παράδειγμα, το οξυγόνο (Ο) μπορεί να σχηματίσει ομοιοπολικούς δεσμούς με τον εαυτό του στο μόριο οξυγόνου (Ο2).
Γενικά, όσο μεγαλύτερη είναι η διαφορά στην ηλεκτροαρνητικότητα μεταξύ δύο στοιχείων, τόσο πιο πιθανό είναι να σχηματίσουν έναν ιοντικό δεσμό.