Ποια είναι η επιστημονική διαδικασία αγωγιμότητας στα μέταλλα;
αγωγιμότητα στα μέταλλα:Μια επιστημονική διαδικασία
Η αγωγιμότητα στα μέταλλα είναι μια συναρπαστική διαδικασία που βασίζεται στη μοναδική δομή και συμπεριφορά των μεταλλικών ατόμων. Ακολουθεί μια ανάλυση των βασικών στοιχείων:
1. Η δομή των μετάλλων:
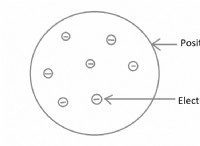
* Δωρεάν ηλεκτρόνια: Σε αντίθεση με άλλα υλικά, τα μέταλλα έχουν μια "θάλασσα" ελεύθερα ηλεκτρόνια. Αυτά τα ηλεκτρόνια δεν συνδέονται με συγκεκριμένα άτομα, αλλά μπορούν να κινούνται ελεύθερα σε όλο το μεταλλικό πλέγμα.
* Μεταλλικό πλέγμα: Τα μεταλλικά άτομα είναι διατεταγμένα σε μια σφιχτά γεμάτη, επαναλαμβανόμενη κρυσταλλική δομή που ονομάζεται μεταλλικό πλέγμα.
2. Ο μηχανισμός αγωγιμότητας:
* Θερμική αγωγιμότητα: Όταν η θερμότητα εφαρμόζεται σε ένα μέταλλο, τα ελεύθερα ηλεκτρόνια απορροφούν την ενέργεια και αρχίζουν να δονείται ταχύτερα. Αυτά τα ενεργοποιημένα ηλεκτρόνια συγκρούονται στη συνέχεια με τα κοντινά ηλεκτρόνια, μεταφέροντας την ενέργειά τους και προκαλώντας τους να δονείται επίσης. Αυτή η διαδικασία συνεχίζεται σε όλο το μέταλλο, μεταφέροντας αποτελεσματικά τη θερμότητα από το ζεστό άκρο στο κρύο άκρο.
* Ηλεκτρική αγωγιμότητα: Όταν ένα ηλεκτρικό πεδίο εφαρμόζεται σε ένα μέταλλο, τα ελεύθερα ηλεκτρόνια προσελκύονται από το θετικό τέλος του πεδίου και απωθούνται από το αρνητικό τέλος. Αυτό προκαλεί καθαρή ροή ηλεκτρονίων, δημιουργώντας ένα ηλεκτρικό ρεύμα.
3. Παράγοντες που επηρεάζουν την αγωγή:
* Θερμοκρασία: Καθώς αυξάνεται η θερμοκρασία, οι θερμικές δονήσεις του μεταλλικού πλέγματος αυξάνονται, καθιστώντας πιο δύσκολο τα ηλεκτρόνια να κινούνται ελεύθερα και να παρεμποδίζουν τόσο τη θερμική όσο και την ηλεκτρική αγωγιμότητα.
* ακαθαρσίες: Η παρουσία ακαθαρσιών σε ένα μέταλλο μπορεί να διαταράξει τη ροή των ηλεκτρονίων, μειώνοντας τόσο τη θερμική όσο και την ηλεκτρική αγωγιμότητα.
* κράμα: Συνδυάζοντας διαφορετικά μέταλλα, μπορούμε να δημιουργήσουμε κράματα με συγκεκριμένες ιδιότητες αγωγιμότητας.
4. Κβαντική Μηχανική Περιγραφή:
* Θεωρία μπάντας: Μια ακριβέστερη περιγραφή της αγωγιμότητας στα μέταλλα προέρχεται από τη θεωρία της μπάντας, η οποία εξηγεί τα ενεργειακά επίπεδα των ηλεκτρονίων σε ένα μέταλλο. Τα ελεύθερα ηλεκτρόνια καταλαμβάνουν μια ζώνη ενεργειακών επιπέδων που ονομάζεται ζώνη αγωγιμότητας, επιτρέποντάς τους να κινούνται εύκολα μέσω του υλικού.
Συνοπτικά:
Η αγωγιμότητα στα μέταλλα είναι αποτέλεσμα της μοναδικής δομής των μετάλλων με ελεύθερα ηλεκτρόνια και η ικανότητα αυτών των ηλεκτρονίων να μεταφέρουν ενέργεια μέσω συγκρούσεων. Αυτή η διαδικασία επηρεάζεται από διάφορους παράγοντες όπως η θερμοκρασία και οι ακαθαρσίες και μπορούν να κατανοηθούν περαιτέρω μέσω της θεωρίας της κβαντικής μηχανικής ζώνης.