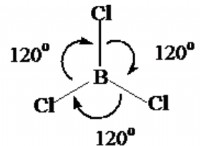
Μήπως τα άτομα επιτυγχάνουν σταθερότητα μετά από ιοντική συγκόλληση στην επιστήμη;
* Κανόνας οκτάδων: Τα άτομα προσπαθούν να επιτύχουν μια σταθερή διαμόρφωση ηλεκτρονίων, που συνήθως μοιάζουν με τη διαμόρφωση ευγενών αερίου με ένα πλήρες εξωτερικό κέλυφος οκτώ ηλεκτρονίων. Αυτό είναι γνωστό ως κανόνας οκτάδων.
* Ιονική σύνδεση: Σε ιοντική συγκόλληση, ένα άτομο (τυπικά ένα μέταλλο) χάνει ηλεκτρόνια για να γίνει ένα θετικά φορτισμένο ιόν (κατιόν), ενώ ένα άλλο άτομο (συνήθως μη μέταλλο) κερδίζει ηλεκτρόνια για να γίνει ένα αρνητικά φορτισμένο ιόν (ανιόν). Αυτή η μεταφορά ηλεκτρονίων επιτρέπει στα δύο άτομα να επιτύχουν ένα σταθερό οκτάτο.
* Ηλεκτροστατική έλξη: Τα αντίθετα φορτισμένα ιόντα προσελκύουν ο ένας τον άλλον, σχηματίζοντας έναν ιοντικό δεσμό. Αυτή η ηλεκτροστατική έλξη συγκρατεί τα ιόντα μαζί σε δομή κρυσταλλικού πλέγματος.
Παραδείγματα:
* Χλωριούχο νάτριο (NaCl): Το νάτριο (Na) χάνει ένα ηλεκτρόνιο για να γίνει Na+, ενώ το χλώριο (CL) κερδίζει ένα ηλεκτρόνιο για να γίνει cl-. Και τα δύο ιόντα έχουν τώρα σταθερές διαμορφώσεις ηλεκτρονίων (όπως το Neon και το Argon, αντίστοιχα). Η προκύπτουσα ηλεκτροστατική έλξη σχηματίζει το χλωριούχο νάτριο ιοντικής ένωσης.
Σημαντική σημείωση:
* Δεν είναι όλα τα άτομα να ακολουθούν τον κανόνα οκτάδων τέλεια. Για παράδειγμα, το υδρογόνο χρειάζεται μόνο δύο ηλεκτρόνια στο εξωτερικό του κέλυφος για να είναι σταθερό.
* Ορισμένα άτομα μπορούν να σχηματίσουν σταθερά ιόντα με λιγότερο ή περισσότερα από οκτώ ηλεκτρόνια στο εξωτερικό τους κέλυφος. Αυτές είναι εξαιρέσεις από τον κανόνα οκτάδων.
Συνοπτικά, η ιοντική συγκόλληση επιτρέπει στα άτομα να επιτευχθούν μια πιο σταθερή ηλεκτρονική διαμόρφωση με την κοινή χρήση ή τη μεταφορά ηλεκτρονίων. Αυτό έχει ως αποτέλεσμα μια πιο σταθερή ένωση με χαμηλότερη κατάσταση ενέργειας.