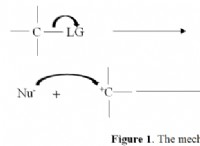
Ποιος είναι ο αριθμός των ηλεκτρονίων που χάνονται ή αποκτήθηκαν που μοιράζονται ένα άτομο κατά τη διάρκεια της πορείας μιας χημικής αντίδρασης;
Δείτε πώς λειτουργεί:
* κατάσταση οξείδωσης είναι μια υποθετική χρέωση που θα είχε ένα άτομο εάν όλοι οι δεσμοί του ήταν 100% ιοντικοί.
* Απώλεια ηλεκτρονίων έχει ως αποτέλεσμα ένα θετικό κατάσταση οξείδωσης.
* κέρδος ηλεκτρονίων έχει ως αποτέλεσμα ένα αρνητικό κατάσταση οξείδωσης.
* Κοινή χρήση ηλεκτρονίων οδηγεί σε ένα μερικό θετική ή αρνητική κατάσταση οξείδωσης, ανάλογα με την ηλεκτροαρνητικότητα των εμπλεκόμενων ατόμων.
Για παράδειγμα:
* νάτριο (na) χάνει ένα ηλεκτρόνιο για να σχηματίσει ένα ιόν νατρίου (Na +) με κατάσταση οξείδωσης +1.
* χλώριο (cl) κερδίζει ένα ηλεκτρόνιο για να σχηματίσει ένα ιόν χλωριούχου (cl-) με κατάσταση οξείδωσης -1.
* Στο νερό (h₂o) , το οξυγόνο (Ο) είναι πιο ηλεκτροαρνητικό από το υδρογόνο (Η), έτσι τραβά τα κοινά ηλεκτρόνια πιο κοντά στον εαυτό του, με αποτέλεσμα ένα μερικό αρνητικό φορτίο στο άτομο οξυγόνου και ένα μερικό θετικό φορτίο στα άτομα υδρογόνου.
Επομένως, ο αριθμός των ηλεκτρονίων που χάθηκαν, αποκτήθηκαν ή μοιράζονται ένα άτομο κατά τη διάρκεια μιας χημικής αντίδρασης είναι ίσος με την αλλαγή στην κατάσταση οξείδωσης.
Σημείωση: Η κατάσταση οξείδωσης είναι μια χρήσιμη έννοια για την κατανόηση των χημικών αντιδράσεων, αλλά είναι σημαντικό να θυμόμαστε ότι είναι μια υποθετική αξία. Η πραγματική κατανομή φορτίου σε ένα μόριο είναι πιο περίπλοκη και μπορεί να επηρεαστεί από παράγοντες όπως η πολικότητα και ο συντονισμός των δεσμών.