Αναμένεται ένα βασικό διάλυμα να περιέχει περισσότερα ιόντα υδρογόνου από τα ιόντα υδροξυλίου;
Εδώ είναι γιατί:
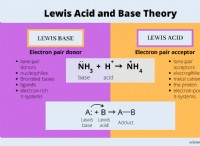
* οξέα έχουν υψηλότερη συγκέντρωση ιόντων υδρογόνου (Η+) από τα ιόντα υδροξυλίου (ΟΗ-).
* βάσεις έχουν υψηλότερη συγκέντρωση ιόντων υδροξυλίου (ΟΗ-) από τα ιόντα υδρογόνου (Η+).
* ουδέτερες λύσεις έχουν ίση συγκέντρωση ιόντων υδρογόνου και υδροξυλίου.
Ως εκ τούτου, μια βασική λύση ορίζεται από την υψηλότερη συγκέντρωση ιόντων υδροξυλίου.