Είναι το διαλυτό χλωριούχο αμμωνίου σε εξάνιο;
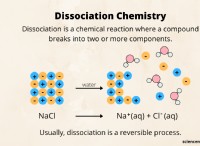
* Polar vs. Nonpolar: Το χλωριούχο αμμώνιο είναι μια ιοντική ένωση, που σημαίνει ότι διαλύεται σε πολικούς διαλύτες. Το Hexane είναι ένας μη πολικός διαλύτης.
* "Όπως διαλύεται όπως": Ο γενικός κανόνας για τη διαλυτότητα είναι "όπως διαλύεται." Οι πολικές ουσίες διαλύονται σε πολικούς διαλύτες και οι μη πολικές ουσίες διαλύονται σε μη πολικούς διαλύτες.
* δεσμός υδρογόνου: Το χλωριούχο αμμώνιο σχηματίζει ισχυρούς δεσμούς υδρογόνου με πολικούς διαλύτες όπως το νερό. Αυτοί οι δεσμοί δεν είναι δυνατοί με μη πολικούς διαλύτες όπως το εξάνιο.
Εν ολίγοις, οι ισχυροί ιοντικοί δεσμοί στο χλωριούχο αμμωνίου και η έλλειψη πολικότητας στην εξάνιο αποτρέπουν οποιαδήποτε σημαντική διάλυση.