Ποιες είναι οι νέες χημικές ουσίες κατά την καύση;
Εδώ είναι μια κατανομή:
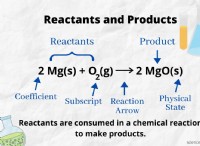
* Αντιδραστήρια: Οι αρχικές ουσίες που καίγονται (π.χ. ξύλο, καύσιμο, χαρτί).
* Προϊόντα: Οι νέες ουσίες που δημιουργήθηκαν κατά τη διάρκεια της διαδικασίας καύσης.
Κοινά προϊόντα καύσης:
* διοξείδιο του άνθρακα (CO2): Ένα άχρωμο, άοσμο αέριο που παράγεται από την καύση καυσίμων με βάση τον άνθρακα.
* νερό (H2O): Σχηματίζεται όταν το υδρογόνο στα αντιδραστήρια συνδυάζεται με οξυγόνο.
* τέφρα: Στερεά υπολείμματα που έμειναν πίσω μετά από καύση, που αποτελείται από ανόργανα υλικά που δεν έκαψαν.
* Καπνός: Ένα μείγμα λεπτών σωματιδίων, αερίων και ατμών που απελευθερώνονται κατά τη διάρκεια της καύσης, που συχνά περιέχουν άκαυστα καύσιμα και άλλα υποπροϊόντα.
Σημείωση: Τα συγκεκριμένα προϊόντα καύσης εξαρτώνται από τις ουσίες που καίγονται και τις συνθήκες της φωτιάς. Ορισμένες πυρκαγιές μπορούν να παράγουν τοξικά αέρια όπως μονοξείδιο του άνθρακα (CO), οξείδια αζώτου (NOX) και διοξείδιο του θείου (SO2).