Ποια αέρια θα εξαλείψουν την ταχύτερα αμμωνία υδρογόνου χλωρίου ή βρωμίου;
Ο νόμος περί συλλογής του Graham
Ο νόμος του Graham δηλώνει ότι ο ρυθμός έκχυσης ενός αερίου είναι αντιστρόφως ανάλογος προς την τετραγωνική ρίζα της μοριακής μάζας του. Με άλλα λόγια, τα ελαφρύτερα αέρια αποβάλλουν ταχύτερα από τα βαρύτερα αέρια.
μοριακές μάζες
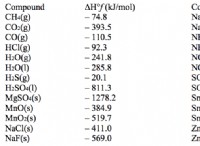
* Χλώριο (CL₂): 35.45 g/mol * 2 =70.90 g/mol
* υδρογόνο (h₂): 1.008 g/mol * 2 =2.016 g/mol
* αμμωνία (NH₃): 14.01 g/mol + (1.008 g/mol * 3) =17.03 g/mol
* Βρωμίνη (BR₂): 79,90 g/mol * 2 =159,80 g/mol
Συμπέρασμα
Δεδομένου ότι το υδρογόνο έχει τη χαμηλότερη μοριακή μάζα, θα αποβάλει τα πιο γρήγορα.
Τάξη των ποσοστών συλλογής (ταχύτερα στην επιβράδυνση):
1. Υδρογόνο (h₂)
2. αμμωνία (NH₃)
3. Χλώριο (CL₂)
4. Βρωμίνη (BR₂)