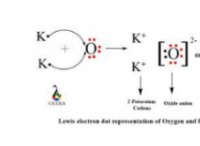
Γιατί είναι ένα ουδέτερο άτομο άνθρακα;
* Διαμόρφωση ηλεκτρονίων: Ο άνθρακας έχει 6 ηλεκτρόνια. Η διαμόρφωσή του ηλεκτρονίων είναι 1S2S²2P2. Αυτό σημαίνει ότι έχει 4 ηλεκτρόνια στο εξώτατο κέλυφος (ηλεκτρόνια σθένους).
* Ηλεκτροργατιστικότητα: Ο άνθρακας είναι μέτρια ηλεκτροαρνητική, που σημαίνει ότι έχει μέτρια τάση να προσελκύει ηλεκτρόνια.
* δεσμός: Ο άνθρακας συχνά σχηματίζει ομοιοπολικούς δεσμούς, μοιράζοντας ηλεκτρόνια με άλλα άτομα. Ωστόσο, λόγω της ηλεκτροαρνητικότητάς του, τείνει να προσελκύει τα κοινόχρηστα ηλεκτρόνια ελαφρώς περισσότερο από τα άτομα με τα οποία δεσμεύεται.
* πολικοί ομοιοπολικοί δεσμοί: Αυτό το ελαφρύ αξιοθέατο έχει ως αποτέλεσμα πολικά ομοιοπολικά δεσμούς , όπου το άτομο άνθρακα έχει ελαφρώς θετικό φορτίο (δ+) και το άλλο άτομο έχει ελαφρώς αρνητικό φορτίο (Δ-).
Επομένως, ένα άτομο άνθρακα δεν είναι ουδέτερο. Συνήθως φέρει ένα ελαφρύ θετικό φορτίο λόγω της ηλεκτροαρνητικότητάς του και του τρόπου με τον οποίο σχηματίζει ομοιοπολικούς δεσμούς.