Γιατί η θερμοκρασία μειώνεται όταν περισσότερο οξύ από το αλκαλικό;
1. Συγκέντρωση οξέος και αλκαλίων:
* υψηλή συγκέντρωση: Εάν προσθέσετε ένα ισχυρό οξύ (όπως το υδροχλωρικό οξύ, HCl) σε ένα ισχυρό αλκάλιο (όπως το υδροξείδιο του νατρίου, NaOH), και οι δύο συμπυκνωμένες, πιθανότατα θα δείτε μια αύξηση θερμοκρασίας Λόγω της θερμότητας που απελευθερώνεται κατά τη διάρκεια της αντίδρασης εξουδετέρωσης.
* Χαμηλή συγκέντρωση: Εάν τα διαλύματα είναι αραιά, η θερμότητα που απελευθερώνεται μπορεί να είναι πολύ μικρή για να ανιχνεύσει μια σημαντική αλλαγή θερμοκρασίας.
2. Το συγκεκριμένο οξύ και αλκαλί:
* Ισχυρά οξέα/ισχυρές βάσεις: Αυτές οι αντιδράσεις συνήθως απελευθερώνουν σημαντική ποσότητα θερμότητας, οδηγώντας σε αύξηση της θερμοκρασίας.
* αδύναμα οξέα/αδύναμες βάσεις: Αυτές οι αντιδράσεις απελευθερώνουν λιγότερη θερμότητα και η αλλαγή της θερμοκρασίας μπορεί να είναι ελάχιστη ή ακόμα και ελαφρά μείωση.
3. Μεταβολή της ενθαλπίας εξουδετέρωσης:
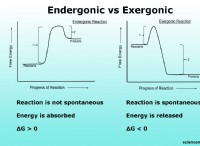
* Εξοθερμική αντίδραση: Εάν η μεταβολή της ενθαλπίας της εξουδετέρωσης είναι αρνητική (δηλ. Η θερμότητα απελευθερώνεται), η θερμοκρασία θα αυξηθεί.
* ενδοθερμική αντίδραση: Εάν η αλλαγή ενθαλπίας είναι θετική (δηλ. Η θερμότητα απορροφάται), η θερμοκρασία θα μειωθεί.
Το σενάριο που περιγράψατε είναι πιθανό το αποτέλεσμα της προσθήκης ενός αραιού οξέος σε μια ισχυρή βάση. Σε αυτή την περίπτωση, η βάση μπορεί να έχει υψηλότερη θερμική ικανότητα, που σημαίνει ότι μπορεί να απορροφήσει περισσότερη θερμότητα χωρίς σημαντική αλλαγή θερμοκρασίας. Η θερμότητα του οξέος μπορεί να απορροφηθεί από τη βάση, προκαλώντας ελαφρά μείωση της θερμοκρασίας.
Παράδειγμα:
Φανταστείτε την προσθήκη μιας σταγόνας αραιό υδροχλωρικό οξύ (HCl) σε μεγάλο όγκο διαλύματος υδροξειδίου του νατρίου (NAOH). Η μικρή ποσότητα θερμότητας που απελευθερώνεται από την αντίδραση εξουδετέρωσης θα απορροφηθεί από τον μεγαλύτερο όγκο βάσης, με αποτέλεσμα μια αμελητέα αλλαγή θερμοκρασίας ή ακόμη και μια ελαφρά μείωση.
Βασικό σημείο: Η μεταβολή της θερμοκρασίας σε μια αντίδραση εξουδετέρωσης εξαρτάται από τις συγκεκριμένες χημικές ουσίες και τις συγκεντρώσεις τους. Δεν είναι ένας κανόνας ότι η προσθήκη περισσότερου οξέος θα οδηγήσει πάντα σε μείωση της θερμοκρασίας.