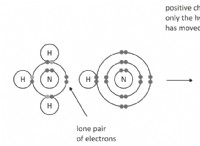
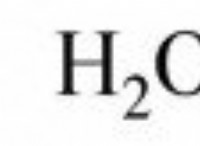Πώς μπορεί να χρησιμοποιηθεί η ηλεκτρόλυση για τον διαχωρισμό του νερού από το υδρογόνο και το οξυγόνο;
Η διαδικασία:
1. Λύση ηλεκτρολύτη: Το ίδιο το νερό είναι ένας φτωχός αγωγός ηλεκτρικής ενέργειας. Για να διευκολυνθεί η διαδικασία, προστίθεται στο νερό μια μικρή ποσότητα ηλεκτρολύτη (όπως αλάτι, οξύ ή βάση). Αυτός ο ηλεκτρολύτης διαλύεται σε ιόντα, καθιστώντας τη λύση αγώγιμη.
2. ηλεκτρόδια: Δύο ηλεκτρόδια (μεταλλικές πλάκες) βυθίζονται στο διάλυμα ηλεκτρολύτη. Ένα ηλεκτρόδιο συνδέεται με το θετικό τερματικό μιας πηγής τροφοδοσίας άμεσης ρεύματος (DC), καθιστώντας το το άνοδο . Το άλλο ηλεκτρόδιο συνδέεται με τον αρνητικό τερματικό, καθιστώντας το το κάθοδο .
3. ηλεκτρόλυση: Όταν ενεργοποιείται η πηγή ισχύος DC, εμφανίζονται οι ακόλουθες αντιδράσεις:
* Στην άνοδο (θετικό ηλεκτρόδιο): Τα μόρια νερού χάνουν ηλεκτρόνια, σχηματίζοντας ιόντα αερίου οξυγόνου και υδρογόνου:
`` `
2H₂O → O₂ + 4H⁺ + 4E⁻
`` `
* Στην κάθοδο (αρνητικό ηλεκτρόδιο): Τα ιόντα υδρογόνου κερδίζουν ηλεκτρόνια, σχηματίζοντας αέριο υδρογόνου:
`` `
4H⁺ + 4E⁻ → 2H₂
`` `
4. Συλλογή: Το αέριο οξυγόνου που παράγεται στην άνοδο συλλέγεται στην κορυφή του κυττάρου, ενώ το αέριο υδρογόνου που παράγεται στην κάθοδο συλλέγεται στο άλλο άκρο.
Γιατί λειτουργεί:
* ηλεκτροχημικές αντιδράσεις: Το ηλεκτρικό ρεύμα παρέχει την ενέργεια που απαιτείται για να σπάσει τους χημικούς δεσμούς στα μόρια του νερού.
* Αντιδράσεις οξειδοαναγωγής: Η ηλεκτρόλυση περιλαμβάνει οξείδωση (απώλεια ηλεκτρονίων) στην άνοδο και τη μείωση (κέρδος των ηλεκτρονίων) στην κάθοδο.
* αποσύνθεση: Η διαδικασία αποσυνδέει το νερό στα συστατικά του στοιχεία, το υδρογόνο και το οξυγόνο.
Σκέψεις ασφάλειας:
* Εκρηκτικό μείγμα: Το υδρογόνο και το οξυγόνο είναι εξαιρετικά εύφλεκτα. Τα αέρια πρέπει να συλλέγονται ξεχωριστά και να χειρίζονται με προσοχή.
* ηλεκτρολύτης: Ο τύπος του χρησιμοποιούμενου ηλεκτρολύτη μπορεί να επηρεάσει την αντίδραση και την ασφάλεια. Ακολουθήστε πάντα τις κατάλληλες οδηγίες.
Εφαρμογές:
* Παραγωγή καυσίμου υδρογόνου: Η ηλεκτρόλυση είναι μια βασική μέθοδος για την παραγωγή αερίου υδρογόνου, μια πηγή καθαρού καυσίμου.
* Παραγωγή οξυγόνου: Χρησιμοποιείται σε διάφορες βιομηχανικές διαδικασίες και ιατρικές εφαρμογές.
* Έρευνα και εκπαίδευση: Η ηλεκτρόλυση είναι μια θεμελιώδη έννοια στη χημεία και χρησιμοποιείται σε πολλές εκπαιδευτικές διαδηλώσεις.
Επιτρέψτε μου να ξέρω αν θέλετε περισσότερες λεπτομέρειες σχετικά με οποιαδήποτε πτυχή της διαδικασίας!