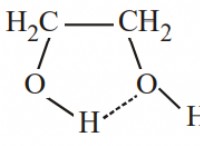
Οι αδύναμοι δεσμοί που σχηματίζουν μια γέφυρα μεταξύ των μορίων νερού καλούνται;
Εδώ είναι γιατί:
* δεσμούς υδρογόνου είναι ένας τύπος διαμοριακής δύναμης (έλξη μεταξύ μορίων) όπου ένα άτομο υδρογόνου προσελκύεται από ένα πολύ ηλεκτροαρνητικό άτομο όπως το οξυγόνο, το άζωτο ή το φθοριοειδές σε άλλο μόριο.
* Στο νερό, το άτομο οξυγόνου είναι πιο ηλεκτροαρνητικό από τα άτομα υδρογόνου, οδηγώντας σε ένα μερικό αρνητικό φορτίο στο οξυγόνο και μερικές θετικές φορτίσεις στα υδρογόνα.
* Αυτό δημιουργεί μια διπολική στιγμή στο μόριο νερού, όπου το θετικό άκρο ενός μορίου μπορεί να αλληλεπιδράσει με το αρνητικό άκρο ενός άλλου, σχηματίζοντας έναν δεσμό υδρογόνου.
Αυτοί οι δεσμοί υδρογόνου είναι ζωτικής σημασίας για πολλές ιδιότητες του νερού, συμπεριλαμβανομένου του υψηλού σημείου βρασμού, της επιφανειακής τάσης και της ικανότητας διαλύσεως πολλών πολικών ουσιών.