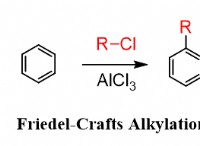
Γιατί οι χημικοί εξισορροπούν τις χημικές εξισώσεις;
Εδώ είναι γιατί η εξισορρόπηση είναι κρίσιμη:
* Τα άτομα δεν δημιουργούνται ή καταστρέφονται: Οι χημικές αντιδράσεις ανακατασκευάζουν τα άτομα, δεν τα δημιουργούν ή καταστρέφουν. Η εξισορρόπηση εξασφαλίζει ότι ο ίδιος αριθμός κάθε τύπου ατόμου εμφανίζεται και στις δύο πλευρές της εξίσωσης, αντανακλώντας αυτή τη θεμελιώδη αρχή.
* Ακριβής αναπαράσταση της πραγματικότητας: Μια ισορροπημένη εξίσωση αντικατοπτρίζει με ακρίβεια την στοιχειομετρία μιας αντίδρασης, που σημαίνει τις ακριβείς αναλογίες των εμπλεκόμενων αντιδραστηρίων και προϊόντων. Αυτό είναι ζωτικής σημασίας για:
* Πρόβλεψη του ποσού των προϊόντων: Γνωρίζοντας πόσο αντιδραστήριο απαιτείται για την παραγωγή μιας συγκεκριμένης ποσότητας προϊόντος.
* Κατανόηση μηχανισμών αντίδρασης: Προσδιορισμός της διαδικασίας βήμα προς βήμα μιας αντίδρασης.
* Απόδοση αντίδρασης υπολογισμού: Προσδιορισμός του πόσα προϊόντα σχηματίζεται πραγματικά σε σύγκριση με το θεωρητικό μέγιστο.
* Ασφάλεια και απόδοση: Οι ισορροπημένες εξισώσεις οδηγούν σε χημικούς για τον προσδιορισμό των σωστών αναλογιών των αντιδραστηρίων για ασφαλείς και αποτελεσματικές αντιδράσεις. Οι μη ισορροπημένες εξισώσεις θα μπορούσαν να οδηγήσουν σε:
* υπερβολικά αντιδραστήρια: Σπαταλώντας υλικά και ενδεχομένως προκαλούν επικίνδυνα υποπροϊόντα.
* Ανεπαρκή αντιδραστήρια: Ατελείς αντιδράσεις, παρεμποδίζοντας το επιθυμητό αποτέλεσμα.
Συνοπτικά, η εξισορρόπηση των χημικών εξισώσεων διασφαλίζει ότι η αναπαράσταση μιας αντίδρασης είναι ακριβής και συνεπής με τους θεμελιώδεις νόμους της χημείας, επιτρέποντας ασφαλείς και αποτελεσματικές χημικές διεργασίες.