Τι είναι η αντίδραση ενυδάτωσης;
Βασικά χαρακτηριστικά μιας αντίδρασης ενυδάτωσης:
* περιλαμβάνει νερό: Το νερό είναι πάντα αντιδραστήριο σε μια αντίδραση ενυδάτωσης.
* Bond Breaking: Το άτομο οξυγόνου του μορίου νερού επιτίθεται σε ένα διπλό ή τριπλό δεσμό μέσα στο μόριο στόχου, σπάζοντας το.
* Νέος σχηματισμός μορίων: Η προσθήκη των ομάδων υδρογόνου και υδροξυλίου του νερού οδηγεί στο σχηματισμό δύο νέων μορίων.
Τύποι αντιδράσεων ενυδάτωσης:
* ενυδάτωση αλκένης: Το νερό προσθέτει σε ένα αλκένιο, σχηματίζοντας αλκοόλ.
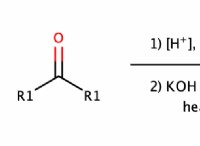
* Alkyne Hydration: Το νερό προσθέτει σε ένα αλκύνι, σχηματίζοντας κετόνη ή αλδεΰδη.
* Ενυδάτωση των carbocations: Το νερό προσθέτει σε ένα carbocation, σχηματίζοντας αλκοόλ.
Παραδείγματα:
1. ενυδάτωση αλκένης: Το αιθένιο (C₂H₄) αντιδρά με νερό για να σχηματίσει αιθανόλη (C₂H₅OH).
`` `
C₂h₄ + h₂o → c₂h₅oh
`` `
2. Alkyne Hydration: Το Propyne (C₃H₄) αντιδρά με νερό για να σχηματίσει προπανόνη (ακετόνη, C₃H₆O).
`` `
C₃h₄ + h₂o → c₃h₆o
`` `
Σημασία των αντιδράσεων ενυδάτωσης:
* Βιομηχανική σύνθεση: Οι αντιδράσεις ενυδάτωσης χρησιμοποιούνται για τη σύνθεση πολλών σημαντικών χημικών ουσιών, συμπεριλαμβανομένων των αλκοόλων, των κετόνων και των αλδεΰδης.
* Βιολογικές διεργασίες: Οι αντιδράσεις ενυδάτωσης διαδραματίζουν κρίσιμο ρόλο σε διάφορες βιολογικές διεργασίες, όπως η πέψη των υδατανθράκων.
* Χημική ανάλυση: Οι αντιδράσεις ενυδάτωσης μπορούν να χρησιμοποιηθούν για τον προσδιορισμό της δομής των μορίων.
Σημείωση: Οι αντιδράσεις ενυδάτωσης απαιτούν συχνά καταλύτες να προχωρήσουν με λογικό ρυθμό. Οι καταλύτες μειώνουν την ενέργεια ενεργοποίησης της αντίδρασης, καθιστώντας ευκολότερη την εμφάνιση της αντίδρασης.