Αντίδραση Wolff–Kishner
Βασικές έννοιες
Σε αυτό το σεμινάριο οργανικής χημείας, θα μάθετε για την αντίδραση αναγωγής Wolff–Kishner και τον μηχανισμό της. Θα δείτε επίσης μερικά παραδείγματα μορίων που υφίστανται τις αναγωγές Wolff–Kishner.
Θέματα που καλύπτονται σε άλλα άρθρα
- Λειτουργική ομάδα καρβονυλίου
- Διαστερεομερή
- Αποχώρηση από τις ομάδες
- Δομές Lewis Dot
- Πυρηνόφιλα
- Δομές συντονισμού
Εισαγωγή στη μείωση Wolff–Kishner
Ο Γερμανός χημικός Ludwig Wolff και ο Ρώσος χημικός Nikolai Kishner ανακάλυψε ανεξάρτητα τη μείωση Wolff–Kishner το 1912 και το 1911, αντίστοιχα.
Στην αναγωγή Wolff–Kishner, μια αλδεΰδη ή μια κετόνη ανάγεται σε αλκάνιο . Πιο συγκεκριμένα, η αναγωγή περιλαμβάνει τη μετατροπή μιαςκαρβονυλικής ομάδας (C=O) σε μια ομάδα μεθυλενίου (–CH2 –).
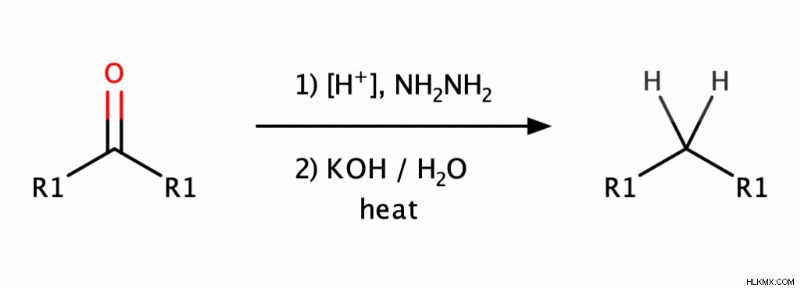
Αυτή η αντίδραση εμφανίζεται σε υψηλές θερμοκρασίες (100–200˚C) και υπό βασικές συνθήκες . Αυτό το κάνει διαφορετικό από τη μείωση του Clemmensen - μια άλλη δημοφιλής αντίδραση μείωσης που εμφανίζεται υπό όξινες συνθήκες. Για να επιλέξει κανείς ποια αντίδραση θα χρησιμοποιήσει, πρέπει να αξιολογήσει την ευαισθησία των υποστρωμάτων του:Η αναγωγή Wolff–Kishner ευνοεί τα ευαίσθητα σε οξύ υποστρώματα, ενώ η μείωση Clemmensen ευνοεί τα ευαίσθητα στη βάση.
Μηχανισμός της μείωσης Wolff–Kishner
Η μείωση Wolff–Kishner περιλαμβάνει δύο βασικά βήματα:τον σχηματισμό υδραζόνης και η αναγωγή της εν λόγω υδραζόνης σε αλκάνιο .
Ο σχηματισμός της υδραζόνης
Υδραζώνες σχηματίζονται όταν υδραζίνες (Ν2 H4 ) αντιδρούν με αλδεΰδες ή κετόνες υπό ήπια όξινο συνθήκες. Σε μια τέτοια αντίδραση, οι υδραζίνες παίζουν το ρόλο ενός πυρηνόφιλου αζώτου .
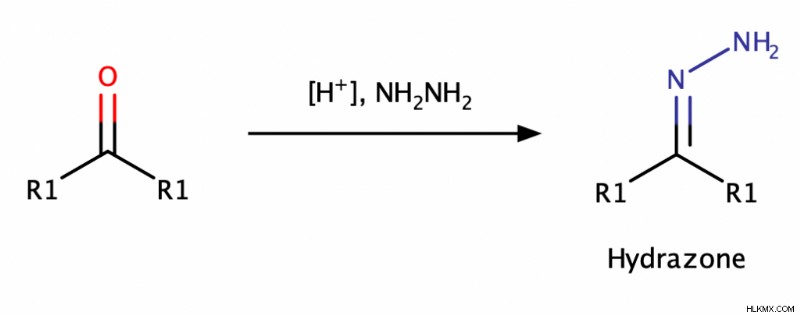
Ο μηχανισμός σχηματισμού της υδραζόνης είναι ο εξής:Πρώτον, ηυδραζίνη εκτελεί μια πυρηνόφιλη επίθεση στο καρβονύλιο ομάδα. Αρκετά βήματα μεταφοράς πρωτονίων που διευκολύνεται από το όξινο περιβάλλον ακολουθούν. Στη συνέχεια, φεύγει το νερό , σχηματίζοντας έναν C=N διπλό δεσμό . Το προκύπτον ενδιάμεσο στη συνέχεια αποπρωτονιώνεται , αποδίδοντας υδραζόνη .
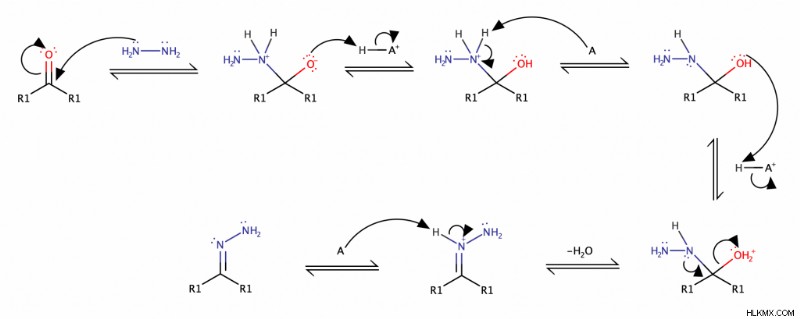
Η Μείωση της Υδραζόνης
Κάτω από βασικές συνθήκες, οι υδραζόνες ανάγεται εύκολα σε αλκάνια—το τελικό προϊόν μιας αντίδρασης αναγωγής Wolff–Kishner.
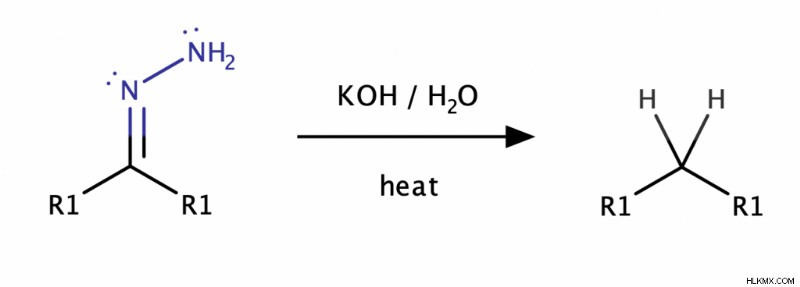
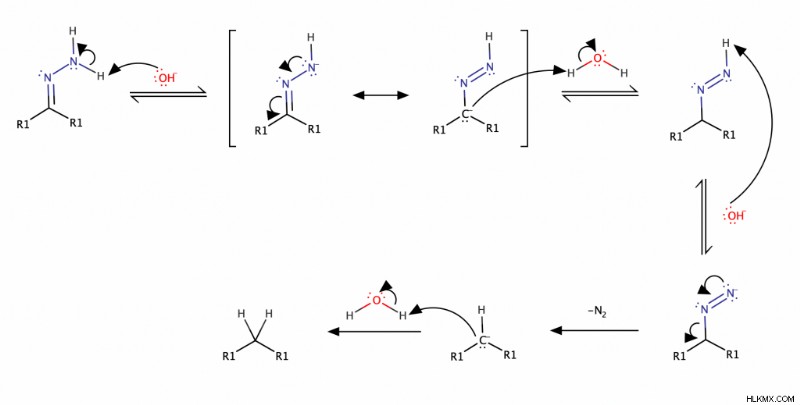
Ο μηχανισμός της αναγωγής της υδραζόνης είναι ο εξής:Πρώτον, τοβασικό περιβάλλον αποπρωτονιώνεται το NH2 της υδραζόνης, σχηματίζοντας ένα σταθεροποιημένο με συντονισμό ενδιάμεσο . Στη συνέχεια, ο αρνητικά φορτισμένος άνθρακας αυτού του ενδιάμεσου πρωτονιώνεται . Αφού η NH χάσει ένα πρωτόνιο, το αέριο άζωτο φεύγει , σχηματίζοντας ένα καρβανιόν (ένας άνθρακας με ένα μη κοινό ζεύγος ηλεκτρονίων). Τέλος, τοκαρμπανιόν είναι πρωτονιωμένο και γίνεταιαλκάνιο .
Είναι σημαντικό να σημειωθεί ότι η αποβολή του αερίου αζώτου έξω από το διάλυμα ως φυσαλίδες αναγκάζει την αντίδραση σε ολοκλήρωση (σύμφωνα με την Αρχή του Le Chatelier), δίνοντας πολύ καλή απόδοση προϊόντος.
Παραδείγματα μειώσεων Wolff–Kishner
Σε αυτό το παράδειγμα, θα μειώσουμε τη βουτανόνη (ή αιθυλομεθυλκετόνη) σε βουτάνιο (ή ν-βουτάνιο). Παρατηρήστε πώς η υδραζόνη έχει δύο διαστερεομερείς μορφές . Αυτό συμβαίνει επειδή η βουτανόνη είναι ασύμμετρη .
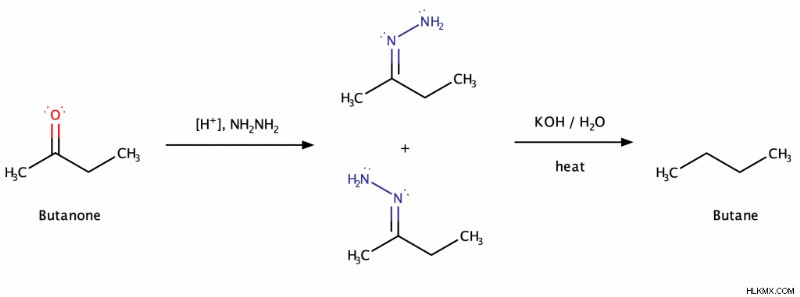
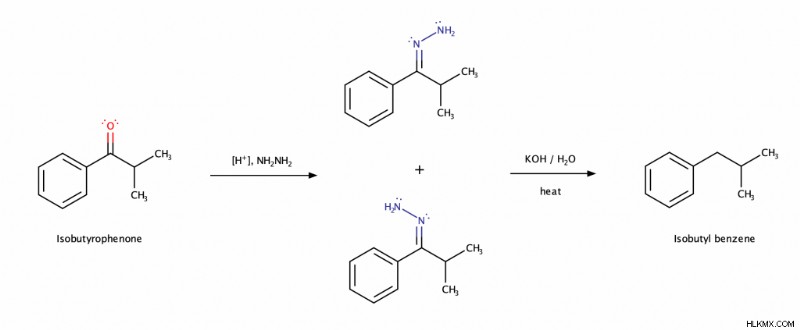
Σε άλλο παράδειγμα, θα μειώσουμε την ισοβουτυροφαινόνη σε ισοβουτυλοβενζόλιο . Παρατηρήστε ξανά πώς η ασυμμετρία της ισοβουτυροφαινόνης έχει ως αποτέλεσμα δύο διαστερεομερή υδραζόνες.
Περαιτέρω ανάγνωση
- Αντίδραση ακυλίωσης Friedel–Crafts
- Αντίδραση Grignard
- Οξυγόνο:Το πιο ευέλικτο στοιχείο
- Στερεοϊσομερή και Χειρικά Κέντρα
- Αντίδραση Wittig