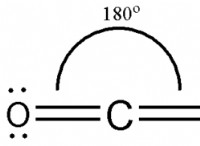
Είναι η φόρμουλα μιας σύνθετης ιοντικής;
* Ιωνικές ενώσεις σχηματίζονται από την ηλεκτροστατική έλξη μεταξύ θετικά φορτισμένων ιόντων (κατιόντων) και αρνητικά φορτισμένων ιόντων (Anions).
* ομοιοπολικές ενώσεις σχηματίζονται από την κοινή χρήση ηλεκτρονίων μεταξύ των ατόμων.
Για να προσδιορίσετε εάν μια ένωση είναι ιοντική, πρέπει να εξετάσετε τα στοιχεία που εμπλέκονται και τις τυπικές συμπεριφορές συγκόλλησης:
* μέταλλα τείνουν να σχηματίζουν κατιόντα (θετικά ιόντα).
* Μη μέταλλα τείνουν να σχηματίζουν ανιόντα (αρνητικά ιόντα).
Εδώ είναι μια γενική κατευθυντήρια γραμμή:
1. Εάν η ένωση περιέχει μέταλλο και μη μέταλλο: Είναι πιθανό μια ιοντική ένωση. Για παράδειγμα:
* NaCl (χλωριούχο νάτριο) - Το νάτριο (Na) είναι ένα μέταλλο, το χλώριο (CL) είναι μη μέταλλο.
* CAO (οξείδιο του ασβεστίου) - Το ασβέστιο (Ca) είναι ένα μέταλλο, το οξυγόνο (Ο) είναι ένα μη μέταλλο.
2. Εάν η ένωση περιέχει μόνο μη μέταλλα: Είναι πιθανό μια ομοιοπολική ένωση. Για παράδειγμα:
* CO2 (διοξείδιο του άνθρακα) - Ο άνθρακας (C) και το οξυγόνο (O) είναι και τα δύο μέταλλα.
* H2O (νερό) - Το υδρογόνο (Η) και το οξυγόνο (Ο) είναι και τα δύο μέταλλα.
Υπάρχουν ορισμένες εξαιρέσεις:
* Πολυατομικά ιόντα: Αυτές είναι ομάδες ατόμων που φέρουν χρέωση και συμπεριφέρονται ως ενιαία μονάδα. Μπορούν να είναι παρόντες τόσο σε ιοντικές όσο και σε ομοιοπολικές ενώσεις. Για παράδειγμα, το χλωριούχο αμμωνίου (NH4CL) είναι ιοντικό, ενώ το διοξείδιο του άνθρακα (CO2) είναι ομοιοπολικό.
Συνοπτικά:
Δεν μπορείτε να προσδιορίσετε εάν μια ένωση είναι ιοντική μόνο κοιτάζοντας τη φόρμουλα της. Πρέπει να εξετάσετε τα στοιχεία που εμπλέκονται και τις τυπικές συμπεριφορές συγκόλλησης. Εάν έχετε τη φόρμουλα, μπορείτε να χρησιμοποιήσετε τον περιοδικό πίνακα και τις γνώσεις σας για ιοντική και ομοιοπολική σύνδεση για να συμπεράνετε τον τύπο της ένωσης.