Πώς αλληλεπιδρούν τα άτομα μεταξύ τους;
1. Ηλεκτροστατικές δυνάμεις:
* έλξη: Οι αντίθετες χρεώσεις προσελκύουν. Αυτό είναι το θεμέλιο της χημικής σύνδεσης. Ο θετικά φορτισμένος πυρήνας ενός ατόμου προσελκύει τα αρνητικά φορτισμένα ηλεκτρόνια ενός άλλου ατόμου.
* Απομάκρυνση: Όπως οι χρεώσεις απωθεί. Τα σύννεφα ηλεκτρονίων των ατόμων απωθούν μεταξύ τους, εμποδίζοντας τα άτομα να φτάσουν πολύ κοντά.
2. Χημική σύνδεση:
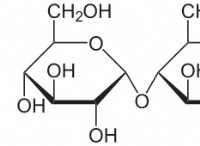
* ομοιοπολική σύνδεση: Τα άτομα μοιράζονται ηλεκτρόνια για να επιτύχουν μια πιο σταθερή διαμόρφωση ηλεκτρονίων. Αυτό έχει ως αποτέλεσμα ισχυρούς δεσμούς και σχηματισμό μορίων.
* Ιονική σύνδεση: Ένα άτομο χάνει ηλεκτρόνια (καθιστώντας θετικά φορτισμένα - κατιόν) ενώ ένα άλλο κερδίζει ηλεκτρόνια (καθιστώντας αρνητικά φορτισμένα - ανιόν). Οι αντίθετες χρεώσεις προσελκύουν στη συνέχεια, σχηματίζοντας ένα ιοντικό δεσμό.
* Μεταλλική σύνδεση: Τα ηλεκτρόνια απομακρύνονται και κινούνται ελεύθερα μεταξύ των ατόμων μετάλλων. Αυτό δημιουργεί έναν ισχυρό δεσμό και εξηγεί τις μοναδικές ιδιότητες των μετάλλων όπως η αγωγιμότητα.
* δεσμός υδρογόνου: Ένας ειδικός τύπος αλληλεπίδρασης διπολικού-δίπολου όπου ένα άτομο υδρογόνου συνδέεται ομοιοπολικά με ένα πολύ ηλεκτροαρνητικό άτομο (όπως το οξυγόνο ή το άζωτο) προσελκύεται από ένα ζεύγος ηλεκτρονίων σε ένα άλλο μόριο.
3. Δυνάμεις Van der Waals:
* αλληλεπιδράσεις διπόλης-διπόλης: Εμφανίζονται μεταξύ πολικών μορίων με μόνιμα διπόλια (ανομοιόμορφη κατανομή των φορτίων).
* Δυνάμεις διασποράς του Λονδίνου: Προσωρινές, κυμαινόμενες διπόλες που προκαλούνται σε μη πολικά μόρια λόγω της κίνησης των ηλεκτρονίων. Αυτά είναι αδύναμα αλλά παρόντα σε όλα τα μόρια.
* δεσμός υδρογόνου (και πάλι): Ενώ ταξινομούνται ως ένας τύπος αλληλεπίδρασης διπολικής-διπόλης, οι δεσμοί υδρογόνου είναι αρκετά ισχυροί ώστε να θεωρούνται ξεχωριστή κατηγορία.
4. Πυρηνικές δυνάμεις:
* Ισχυρή πυρηνική δύναμη: Αυτή η δύναμη συγκρατεί τα πρωτόνια και τα νετρόνια μαζί στον πυρήνα ενός ατόμου. Είναι απίστευτα ισχυρό, αλλά ενεργεί σε πολύ μικρές αποστάσεις.
* Αδύναμη πυρηνική δύναμη: Υπεύθυνος για τη ραδιενεργή αποσύνθεση, αυτή η δύναμη είναι ασθενέστερη από την ισχυρή πυρηνική δύναμη, αλλά ενεργεί σε μεγαλύτερες αποστάσεις.
Οι ενδοατομικές αλληλεπιδράσεις καθορίζουν τις ιδιότητες της ύλης:
* Ο τύπος δεσμού υπαγορεύει τη φυσική κατάσταση (στερεό, υγρό, αέριο) και ιδιότητες μιας ουσίας.
* Οι αδύναμες αλληλεπιδράσεις όπως οι δυνάμεις van der Waals μπορούν να επηρεάσουν τα σημεία τήξης και βρασμού, διαλυτότητα και ακόμη και βιολογικές διεργασίες.
* Οι ισχυρές αλληλεπιδράσεις όπως οι χημικοί δεσμοί καθορίζουν τον σχηματισμό σύνθετων μορίων και υλικών.
Η πολυπλοκότητα των ενδοατομικών αλληλεπιδράσεων εξηγεί την τεράστια σειρά των ουσιών και τις μοναδικές τους ιδιότητες που βλέπουμε στον κόσμο. Η κατανόηση αυτών των αλληλεπιδράσεων είναι θεμελιώδης για τη χημεία, τη φυσική και την επιστήμη των υλικών.