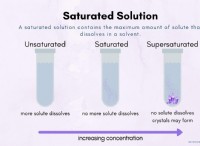
Γιατί η θέρμανση αυξάνει την ταχύτητα με την οποία διαλύεται μια διαλυμένη ουσία στο νερό;
1. Αυξημένη κινητική ενέργεια:
* Περισσότερη κίνηση: Η θερμότητα παρέχει ενέργεια στα μόρια του νερού, προκαλώντας τους να κινούνται ταχύτερα και πιο τυχαία. Αυτή η αυξημένη κινητική ενέργεια τους κάνει να συγκρούονται με τα σωματίδια διαλυτής ουσίας συχνότερα και με μεγαλύτερη δύναμη.
* Breaking Bonds: Οι αυξημένες συγκρούσεις διαταράσσουν τις δυνάμεις που συγκρατούν τα σωματίδια διαλυμένης ουσίας, σπάζοντας τους χωριστά και επιτρέποντάς τους να αλληλεπιδρούν με τα μόρια του νερού.
2. Αυξημένη πολικότητα διαλύτη:
* Αδύνατες αλληλεπιδράσεις: Η θερμότητα αποδυναμώνει τους δεσμούς υδρογόνου μεταξύ των μορίων του νερού, καθιστώντας το νερό λιγότερο "κολλώδες" και επιτρέποντάς του να αλληλεπιδρά πιο εύκολα με τα σωματίδια διαλυμένης ουσίας.
* Καλύτερη διαλυτοποίηση: Αυτή η αυξημένη πολικότητα επιτρέπει στα μόρια του νερού να περιβάλλουν καλύτερα και να διαλύουν τα σωματίδια διαλυτής ουσίας, οδηγώντας σε ταχύτερη διάλυση.
3. Μειωμένο ιξώδες:
* Λιγότερη αντίσταση: Η θέρμανση μειώνει το ιξώδες του νερού, που σημαίνει ότι γίνεται λιγότερο ανθεκτικό στη ροή. Αυτό επιτρέπει στα μόρια του νερού να κινούνται πιο ελεύθερα, διευκολύνοντας την καλύτερη επαφή με τη ουσία.
4. Αυξημένη διαλυτότητα:
* Υψηλότερη συγκέντρωση: Αν και δεν σχετίζεται άμεσα με την * ταχύτητα * της διάλυσης, η θερμότητα συχνά αυξάνει την * ποσότητα * της ουσίας που μπορεί να διαλύεται σε μια δεδομένη ποσότητα νερού. Αυτό οφείλεται στο γεγονός ότι οι υψηλότερες θερμοκρασίες επιτρέπουν περισσότερα σωματίδια διαλυμένης ουσίας να ξεπεράσουν τις δικές τους διαμοριακές δυνάμεις και να εισέλθουν στο διάλυμα.
Συνοπτικά: Η θέρμανση αυξάνει τον ρυθμό διάλυσης αυξάνοντας την κινητική ενέργεια των μορίων του νερού, καθιστώντας τα καλύτερα να σπάσουν τη διαλυτή ουσία και να περιβάλλουν τα σωματίδια του. Ενισχύει επίσης την πολικότητα του νερού, καθιστώντας την πιο αποτελεσματική διαλύτη.