Τι είναι τα γαλβανικά κύτταρα; Μια υπεραπλουστευμένη εξήγηση
Τα γαλβανικά κύτταρα είναι ηλεκτροχημικά στοιχεία που μετατρέπουν τη χημική ενέργεια σε ηλεκτρική ενέργεια. Είναι συμπαγείς πηγές ηλεκτρικής ενέργειας.
ΕΛΑΦΡΟ ΚΤΥΠΗΜΑ! ΕΛΑΦΡΟ ΚΤΥΠΗΜΑ! ΕΛΑΦΡΟ ΚΤΥΠΗΜΑ! "Αυτό το τηλεχειριστήριο σταματά να λειτουργεί μόνο όταν θέλουμε πραγματικά να παρακολουθήσουμε κάτι!" φώναξε ο παππούς του Αρούν καθώς έσπασε το τηλεχειριστήριο της τηλεόρασης στο χέρι του.
«Σταμάτα να το χτυπάς αυτό, μπαμπά, και βάλε πρώτα αυτές τις μπαταρίες», είπε η μαμά του Αρούν. Ο Αρούν είδε τη μητέρα του να παραδίδει δύο αντικείμενα στον παππού του και όταν φόρτωσε στο τηλεχειριστήριο, ξαφνικά λειτούργησε. Ο Arun ήταν έκπληκτος και περίεργος για το τι ήταν και γιατί έπρεπε να αντικατασταθούν.

Δεν είναι αυτό ένα από τα πιο συνηθισμένα σενάρια σε ένα νοικοκυριό; Όπως ο Arun, οι περισσότεροι από εμάς ως παιδιά θα αναρωτιόμασταν τι ήταν οι μπαταρίες. Μερικοί από εμάς μπορεί να προσπάθησαν ακόμη και να τα σπάσουν, απλώς για να δουν τι υπήρχε μέσα σε αυτό το άκαμπτο, δύσκολο να σπάσει κέλυφος!
Τι είναι η μπαταρία;
Οι μπαταρίες είναι απλώς μια πηγή ηλεκτρικής ενέργειας . Συνδέουμε τις συσκευές μας σε πρίζες για να πάρουν ρεύμα και να λειτουργήσουν. Ομοίως, οι μπαταρίες είναι συμπαγείς πηγές ηλεκτρικής ενέργειας. Μια μπαταρία είναι ένα πακέτο από ένα ή περισσότερα γαλβανικά στοιχεία που παράγει ρεύμα με τη χρήση χημικών.
Τώρα, τι είναι τα γαλβανικά κύτταρα;
Για να το κατανοήσουμε καλύτερα, ας δημιουργήσουμε έναν μικρό κόσμο για να μάθουμε τι είναι και πώς παράγουν ηλεκτρική ενέργεια.
Κατανόηση των γαλβανικών στοιχείων μέσω μιας γαλβανικής αυτοκρατορίας
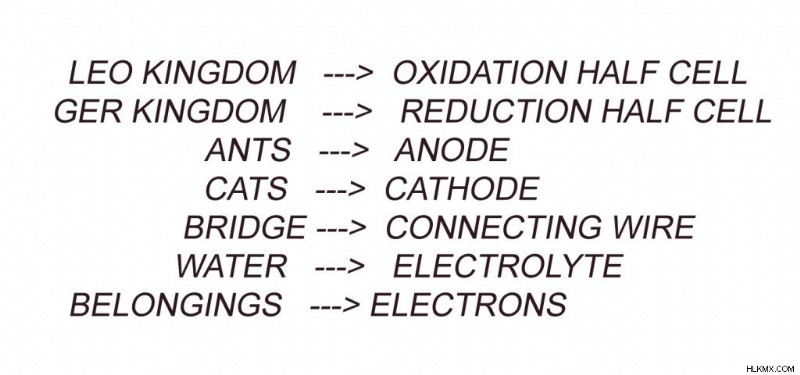
Πολύ καιρό πριν υπήρχε μια αυτοκρατορία που ονομαζόταν Γαλβανική Αυτοκρατορία. Αποτελούνταν από δύο βασίλεια που ονομάζονταν το βασίλειο LEO και το βασίλειο GER. Οι άνθρωποι του βασιλείου LEO ονομάζονταν Μυρμήγκια και οι άνθρωποι του βασιλείου GER ονομάζονταν Γάτες .
Και τα δύο βασίλεια χωρίστηκαν και περιβάλλονταν από νερό και τεράστια τείχη.
Ωστόσο, τα δύο βασίλεια δεν μπορούσαν να λειτουργήσουν χωριστά. Έπρεπε να συνεργαστούν για να διατηρήσουν μια επιτυχημένη και ειρηνική αυτοκρατορία. Η ενότητα είναι το κλειδί! Ως εκ τούτου, τα βασίλεια συνδέονταν με μια γέφυρα για να επικοινωνούν και να μεταφέρουν υλικά μεταξύ τους.
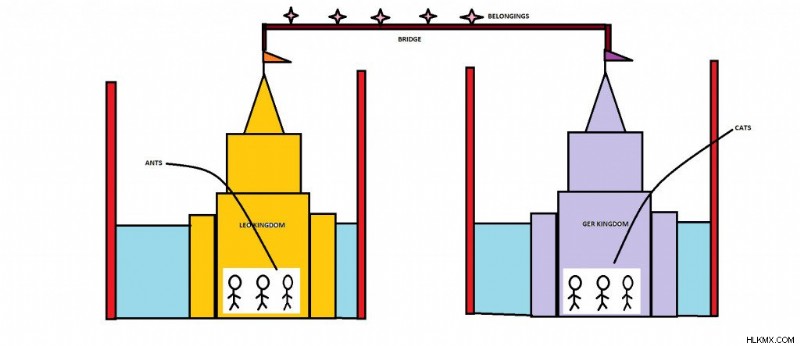
Η ΓΑΛΒΑΝΙΚΗ ΑΥΤΟΚΡΑΤΟΡΙΑ
Μια αξιοσημείωτη ιδιότητα των Μυρμηγκιών, δηλαδή των ανθρώπων του LEO, είναι ότι θυσιάζονται. Χάνουν ή θυσιάζουν τα «υπάρχοντά» τους στις Γάτες. Και αυτά τα «Αντικείμενα» μεταφέρονται μέσω της συνδετικής γέφυρας. Η αξιοσημείωτη ιδιότητα μεταξύ των Cats, δηλαδή των ανθρώπων του βασιλείου GER, είναι ότι είναι αποκτητές. Αποδέχονται τα «πράγματα» που δίνουν τα Μυρμήγκια.
Όσο περισσότερο θυσιάζει το βασίλειο LEO, τόσο περισσότερο μεγαλώνει το βασίλειο του GER. Λυπηρό, αλλά αληθινό!
Τα μυρμήγκια συρρικνώνονται ενώ οι γάτες μεγαλώνουν.
Όπως μπορεί να μαντέψει ο καθένας, κάποια στιγμή θα υπάρξουν λιγότερα «πράγματα» για να δώσουν τα Μυρμήγκια και για να κερδίσουν οι Γάτες. Ως εκ τούτου, οι αυτοκρατορίες θα σταματήσουν να λειτουργούν.
Αυτή είναι η άνοδος και η πτώση των Γαλβανικών Αυτοκρατοριών!
Ας το βάλουμε στην επιστήμη!
Τώρα ας το μεταφράσουμε στον πραγματικό κόσμο με τη βοήθεια αυτής της μικρής αυτοκρατορίας που δημιουργήσαμε.
Ένα γαλβανικό κελί αποτελείται από 2 μισά κελιά (αναφέρονται ως βασίλεια). το ημικύτταρο οξείδωσης (βασίλειο LEO) και το ημικύτταρο Αναγωγής (Βασίλειο GER).
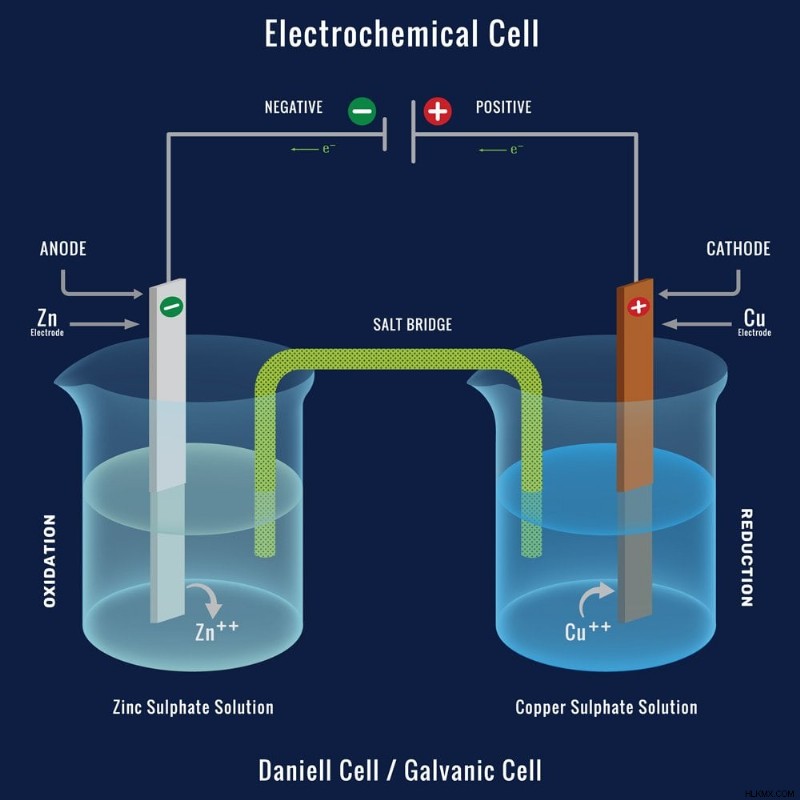
Ένα γαλβανικό κελί (Φωτογραφία:Nandalal Sarkar/Shutterstock)
Κάθε μισό στοιχείο αποτελείται από ένα μέταλλο (άνθρωποι) βουτηγμένο σε έναν ηλεκτρολύτη (Νερό). Αυτά τα δύο μισά κελιά συνδέονται με ένα καλώδιο (τη γέφυρα). Σε ένα από τα μέταλλα γίνεται η απώλεια ηλεκτρονίων (θυσία), ενώ το άλλο μέταλλο κερδίζει (Αποκτά) ηλεκτρόνια. Αυτά τα ηλεκτρόνια μεταφέρονται μέσω του καλωδίου σύνδεσής μας.
Το μέταλλο όπου λαμβάνει χώρα η οξείδωση (απώλεια ηλεκτρονίων) ονομάζεται άνοδος (Μυρμήγκια) και το μέταλλο όπου λαμβάνει χώρα η αναγωγή (Κέρδος ηλεκτρονίων) ονομάζεται Κάθοδος (Γάτες). Η οξείδωση και η αναγωγή δεν μπορούν να πραγματοποιηθούν χωριστά.
Ο ψευδάργυρος και ο χαλκός χρησιμοποιούνται συνήθως ως δύο ηλεκτρόδια βουτηγμένα σε διαλύματα θειικού ψευδαργύρου και θειικού χαλκού, αντίστοιχα. Ο Zn χάνει ηλεκτρόνια και γίνεται Zn2+ (Οξείδωση), ενώ το Cu2+ στο διάλυμα θειικού χαλκού κερδίζει αυτά τα ηλεκτρόνια και γίνεται Cu.
Η Άνοδος διαβρώνεται, ενώ η κάθοδος μεγαλώνει. Όπως γνωρίζουμε ήδη, η κίνηση αυτών των ηλεκτρονίων αναφέρεται ως ρεύμα ή ηλεκτρισμός. Αυτή είναι η απλή λειτουργία του γαλβανικού κυττάρου.
Πώς θυμάμαι;
Είναι λίγο μπερδεμένο να θυμόμαστε, όπου είναι χρήσιμα τα αρκτικόλεξά μας.

Η απώλεια ηλεκτρονίων ονομάζεται οξείδωση ενώ το κέρδος ηλεκτρονίων ονομάζεται αναγωγή .
Εάν μια συσκευή που απαιτεί ρεύμα, όπως ένας λαμπτήρας, τοποθετηθεί ανάμεσα στο καλώδιο σύνδεσης, αυτό ανάβει λόγω της ροής ηλεκτρονίων. Έτσι λειτουργεί το Γαλβανικό στοιχείο ως πηγή ηλεκτρικής ενέργειας.
Συμπέρασμα
Η ιδέα ότι δύο μέταλλα, όταν έρθουν σε επαφή, μπορούν να παράγουν ηλεκτρισμό, ανακαλύφθηκε από τον Luigi Galvani. Όταν δύο διαφορετικά μέταλλα ήταν σε επαφή και όταν και τα δύο ακουμπήθηκαν ταυτόχρονα σε δύο διαφορετικά μέρη ενός μυός στο πόδι ενός βατράχου, για να κλείσει το κύκλωμα, το πόδι του βατράχου συσπάστηκε.
Ένα χρόνο μετά τη δημοσίευση του έργου του Galvani (1790), ο Alessandro Volta έδειξε ότι ο βάτραχος δεν ήταν απαραίτητος, χρησιμοποιώντας αντ 'αυτού έναν ανιχνευτή με βάση τη δύναμη και χαρτί εμποτισμένο με άλμη (ως ηλεκτρολύτη). Ως εκ τούτου, οι όροι Γαλβανικά κύτταρα και Βολταϊκά στοιχεία είναι συχνά εναλλάξιμα και αναφέρονται στην ίδια εγκατάσταση.
Οι γαλβανικές κυψέλες έχουν μεγάλη ποικιλία εφαρμογών και χρησιμοποιούνται σε ρολόγια, ρολόγια, τηλεχειριστήρια, τηλέφωνα, κάμερες, φορητούς υπολογιστές και πολλά άλλα κοινά αντικείμενα. Το ότι είναι ελαφρύ, φορητό και επαναφορτιζόμενο είναι μερικά από τα βασικά πλεονεκτήματα των κυψελών Galvanic, τα οποία έχουν αλλάξει τον τρόπο με τον οποίο τροφοδοτούμε τη ζωή μας με αμέτρητους τρόπους!