Ποια ατομικά σωματίδια είναι πιο σημαντικά για τον προσδιορισμό των χημικών αντιδράσεων και γιατί;
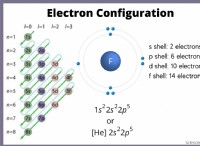
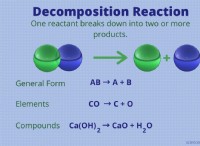
* Τα ηλεκτρόνια εμπλέκονται στη συγκόλληση: Οι χημικές αντιδράσεις εμφανίζονται όταν τα άτομα αλληλεπιδρούν μεταξύ τους, σχηματίζοντας ή σπάζοντας χημικούς δεσμούς. Αυτοί οι δεσμοί σχηματίζονται κυρίως από την κοινή χρήση ή τη μεταφορά ηλεκτρονίων μεταξύ των ατόμων.
* Τα ηλεκτρόνια καθορίζουν την αντιδραστικότητα: Η διάταξη των ηλεκτρονίων σε ένα εξωτερικό κέλυφος ενός ατόμου (ηλεκτρόνια σθένους) υπαγορεύει πώς ένα άτομο θα αλληλεπιδρά με άλλα άτομα. Τα άτομα με υψηλό αριθμό ηλεκτρόνων σθένους τείνουν να είναι λιγότερο αντιδραστικά, ενώ εκείνα με χαμηλό αριθμό ηλεκτρόνων σθένους είναι πιο αντιδραστικά.
* Τα ηλεκτρόνια εμπλέκονται στη μεταφορά ενέργειας: Οι χημικές αντιδράσεις περιλαμβάνουν την απορρόφηση ή την απελευθέρωση ενέργειας. Αυτή η ενέργεια συχνά αποθηκεύεται ή απελευθερώνεται με τη μορφή αλλαγών στα ενεργειακά επίπεδα των ηλεκτρονίων εντός ατόμων και μορίων.
Ενώ τα πρωτόνια και τα νετρόνια είναι σημαντικά για τον ορισμό της ταυτότητας ενός στοιχείου και της μάζας του, δεν συμμετέχουν άμεσα στο σχηματισμό ή το σπάσιμο των χημικών δεσμών. Τα πρωτόνια καθορίζουν τον ατομικό αριθμό ενός στοιχείου, ο οποίος καθορίζει την ταυτότητά του. Τα νετρόνια συμβάλλουν στη μάζα ενός ατόμου και μπορούν να επηρεάσουν τη σταθερότητά του μέσω των ισότοπων.
Συνοπτικά: Τα ηλεκτρόνια είναι οι κύριοι παράγοντες των χημικών αντιδράσεων επειδή εμπλέκονται στη συγκόλληση, καθορίζουν την αντιδραστικότητα ενός ατόμου και συμμετέχουν στη μεταφορά ενέργειας κατά τη διάρκεια των αντιδράσεων.