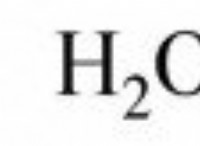Τι μας λέει η δομή ενός μεθανίου μορίου;
1. Σχήμα και συγκόλληση:
* Tetrahedral: Το μεθάνιο έχει τετραεδρικό σχήμα, που σημαίνει ότι το άτομο άνθρακα βρίσκεται στο επίκεντρο ενός τετράεδρου, με τέσσερα άτομα υδρογόνου στις γωνίες. Αυτό το σχήμα οφείλεται στα τέσσερα sp
* Ισχυρά ομόλογα C-H: Οι δεσμοί C-H είναι πολύ ισχυροί και μη πολικοί. Αυτό συμβάλλει στη σταθερότητα του μεθανίου και στη χαμηλή αντιδραστικότητα.
2. Πολικότητα και διαλυτότητα:
* Nonpolar: Λόγω του συμμετρικού σχήματος και των μη πολικών δεσμών C-H, το μεθάνιο είναι ένα μη πολικό μόριο. Αυτό σημαίνει ότι δεν έχει θετικό ή αρνητικό τέλος και δεν διαλύεται εύκολα σε πολικούς διαλύτες όπως το νερό.
* Χαμηλή διαλυτότητα στο νερό: Η μη πολωτικότητα του μεθανίου το καθιστά πολύ κακώς διαλυτή στο νερό. Αυτό οφείλεται στο γεγονός ότι τα μόρια του νερού είναι πολικά και αλληλεπιδρούν έντονα μεταξύ τους, ενώ τα μόρια μεθανίου δεν το κάνουν.
3. Γωνίες σύνδεσης:
* 109,5 μοίρες: Οι γωνίες δεσμού μεταξύ του ατόμου άνθρακα και κάθε ατόμου υδρογόνου είναι 109,5 μοίρες. Αυτή η συγκεκριμένη γωνία συμβάλλει στη σταθερότητα και το σχήμα του μορίου.
4. Χημική συμπεριφορά:
* καύση: Το μεθάνιο είναι εξαιρετικά εύφλεκτο και εύκολα υποβάλλεται σε καύση με οξυγόνο για να σχηματίσει διοξείδιο του άνθρακα (Co
* σχετικά αδρανές: Το μεθάνιο είναι σχετικά αδρανές, που σημαίνει ότι δεν αντιδρά με πολλές άλλες ουσίες. Τα σταθερά ομόλογα C-H καθιστούν δύσκολη τη διάσπαση.
5. Φυσικές ιδιότητες:
* αέριο σε θερμοκρασία δωματίου: Λόγω του χαμηλού μοριακού βάρους και των αδύναμων διαμοριακών δυνάμεων, το μεθάνιο είναι ένα αέριο σε θερμοκρασία δωματίου.
* Χαμηλό σημείο βρασμού: Οι αδύναμες διαμοριακές δυνάμεις μεταξύ των μορίων μεθανίου έχουν ως αποτέλεσμα ένα χαμηλό σημείο βρασμού (-161,5 ° C).
Συνοπτικά: Η τετραεδρική δομή του μεθανίου, η μη πολική της, οι ισχυροί δεσμοί C-H και οι ειδικές γωνίες δεσμών συμβάλλουν στις σημαντικές ιδιότητες και τις εφαρμογές του ως καύσιμο και συστατικό του φυσικού αερίου.