Τι θα εξουδετερώσει τη διάβρωση του αλμυρού αλουμινίου;
Κατανόηση του προβλήματος:
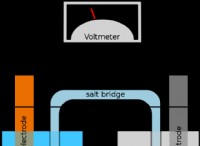
* Ηλεκτροχημική αντίδραση: Η διάβρωση του αλμυρού αλουμινίου συμβαίνει λόγω ηλεκτροχημικής αντίδρασης. Το αλουμίνιο σχηματίζει ένα προστατευτικό στρώμα οξειδίου, αλλά το αλμυρό νερό διαταράσσει αυτό το στρώμα, οδηγώντας σε οξείδωση (σκουριά).
* Γαλβανική διάβρωση: Εάν το αλουμίνιο έρχεται σε επαφή με άλλα μέταλλα (όπως χάλυβα ή ορείχαλκο) σε αλμυρό νερό, συμβαίνει γαλβανική διάβρωση. Αυτό είναι όπου το πιο ενεργό μέταλλο (αλουμίνιο) διαβρώνεται ταχύτερα λόγω της ροής ηλεκτρικού ρεύματος.
Πρόληψη και μετριασμός:
1. Προστατευτικά επικαλύψεις:
* Ανδόζη: Αυτό δημιουργεί ένα παχύτερο, πιο ανθεκτικό στρώμα οξειδίου στην επιφάνεια του αλουμινίου.
* Επικάλυψη σκόνης: Μια ανθεκτική, χημικά ανθεκτική επικάλυψη που μπορεί να εφαρμοστεί σε διάφορα χρώματα.
* βαφή: Το σωστά εφαρμοσμένο θαλάσσιο χρώμα μπορεί να δώσει ένα εμπόδιο κατά του αλμυρού νερού.
2. Επιλογή υλικού:
* Αλουμίνιο θαλάσσιας ποιότητας: Κράματα αλουμινίου που έχουν σχεδιαστεί για αντίσταση σε περιβάλλοντα αλμυρού νερού.
* ανοξείδωτος χάλυβα: Εάν πρέπει να χρησιμοποιήσετε ένα άλλο μέταλλο, σκεφτείτε ανοξείδωτο χάλυβα, ο οποίος είναι πιο ανθεκτικός στη διάβρωση.
3. Σχεδιασμός Σχεδιασμός:
* Αποφύγετε τα σημεία επαφής: Ελαχιστοποιήστε την επαφή μεταξύ των ανόμοιων μετάλλων για τη μείωση της γαλβανικής διάβρωσης.
* Αποστράγγιση: Εξασφαλίστε την κατάλληλη αποστράγγιση για την πρόληψη της συγκέντρωσης νερού και της εκτεταμένης έκθεσης.
4. Τακτική συντήρηση:
* Καθαρισμός: Ξεπλύνετε τακτικά τις αποθέσεις αλατιού για να ελαχιστοποιήσετε τη διάβρωση.
* Επιθεώρηση: Ελέγξτε για τα σημάδια της διάβρωσης νωρίς και τα αντιμετωπίστε αμέσως.
Σημαντικές σημειώσεις:
* Όχι "εξουδετέρωση" :Μόλις ξεκινήσει η διάβρωση, είναι δύσκολο να αντιστραφεί. Εστίαση στην πρόληψη και επιβράδυνση της διαδικασίας.
* σωστή εφαρμογή: Η αποτελεσματικότητα οποιασδήποτε λύσης εξαρτάται από την κατάλληλη εφαρμογή της. Συμβουλευτείτε τους επαγγελματίες για συγκεκριμένες εφαρμογές και καθοδήγηση.
Παράδειγμα:
Εάν έχετε ένα σκάφος σκάφους αλουμινίου, θα μπορούσατε να χρησιμοποιήσετε ένα συνδυασμό μεθόδων:
* Αλουμίνιο θαλάσσιας ποιότητας: Επιλέξτε ένα κύτος κατασκευασμένο από θαλάσσιο αλουμίνιο.
* Ανδόζη: Ανοδικά το κύτος για επιπλέον προστασία.
* Marine Paint: Εφαρμόστε ένα θαλάσσιο χρώμα υψηλής ποιότητας πάνω από την ανοδίωση.
* Τακτικός καθαρισμός: Ξεπλύνετε το κύτος με γλυκό νερό μετά από κάθε χρήση για να αφαιρέσετε τις αποθέσεις αλατιού.
Λαμβάνοντας αυτά τα βήματα, μπορείτε να ελαχιστοποιήσετε σημαντικά τη διάβρωση του αλμυρού νερού του σκάφους αλουμινίου σας.