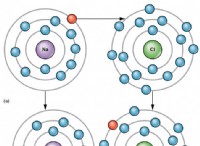
Τι συμβαίνει με τα άτομα σε μια αντίδραση μετατόπισης;
* Αντιδραστήρια: Η αντίδραση ξεκινά με δύο αντιδραστήρια:
* Ένα πιο αντιδραστικό στοιχείο (συνήθως ένα μέταλλο)
* Μια ένωση που περιέχει ένα λιγότερο αντιδραστικό στοιχείο (συχνά ένα μέταλλο).
* Το "swap": Το πιο αντιδραστικό στοιχείο μετατοπίζει το λιγότερο αντιδραστικό στοιχείο από την ένωση. Αυτό σημαίνει ότι το πιο δραστικό στοιχείο σχηματίζει μια νέα ένωση με το ανιόν από την αρχική ένωση, ενώ το λιγότερο αντιδραστικό στοιχείο απελευθερώνεται ως ελεύθερο στοιχείο.
* νέα προϊόντα: Το αποτέλεσμα είναι δύο νέα προϊόντα:
* Μια νέα ένωση που σχηματίζεται από το πιο αντιδραστικό στοιχείο και το ανιόν από την αρχική ένωση.
* Το λιγότερο αντιδραστικό στοιχείο υπάρχει τώρα ως ελεύθερο στοιχείο.
Παράδειγμα:
Εξετάστε την αντίδραση μεταξύ του μεταλλικού ψευδαργύρου (Zn) και του διαλύματος θειικού χαλκού (CUSO₄).
* Αντιδραστήρια: Ο ψευδάργυρος (Zn) είναι πιο αντιδραστικός από τον χαλκό (Cu).
* μετατόπιση: Ο ψευδάργυρος μετατοπίζει χαλκό από τη θειική ένωση.
* Προϊόντα: Το θειικό ψευδάργυρο (ZnSO₄) σχηματίζεται και ο χαλκός (Cu) απελευθερώνεται ως συμπαγής χαλκός.
Εξίσωση:
Zn (s) + cuso₄ (aq) → znso₄ (aq) + cu (s)
Βασικά σημεία:
* καμία αλλαγή στον αριθμό των ατόμων: Τα άτομα απλά αναδιαμορφώνονται, δεν δημιουργούνται ή καταστρέφονται. Αυτό ακολουθεί το νόμο της διατήρησης της μάζας.
* Τα ηλεκτρόνια μεταφέρονται: Το πιο αντιδραστικό στοιχείο χάνει ηλεκτρόνια (οξείδωση) και το λιγότερο αντιδραστικό στοιχείο κερδίζει ηλεκτρόνια (μείωση).
* Σειρά αντιδραστικότητας: Η αντιδραστικότητα των μετάλλων καθορίζεται από την τάση τους να χάσουν ηλεκτρόνια. Ένα πιο αντιδραστικό μέταλλο θα μετατοπίσει ένα λιγότερο αντιδραστικό μέταλλο από την ένωση του.
Επιτρέψτε μου να ξέρω αν θέλετε να εξερευνήσετε συγκεκριμένα παραδείγματα ή να έχετε περαιτέρω ερωτήσεις!