Πώς είναι παρόμοιες οι δομές ηλεκτρονίων του βορίου (b) και του αλουμινίου (AL);
* ηλεκτρόνια σθένους: Τόσο το βόριο όσο και το αλουμίνιο έχουν τρία ηλεκτρόνια σθένους στο εξωτερικό επίπεδο ενέργειας τους. Αυτό είναι το καθοριστικό χαρακτηριστικό των στοιχείων της ομάδας 13.
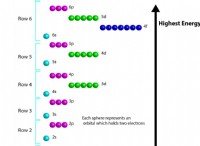
* Διαμόρφωση ηλεκτρονίων: Οι διαμορφώσεις ηλεκτρονίων τους μοιράζονται ένα κοινό μοτίβο:
* Boron:1S² 2S2 2P¹
* Αλουμίνιο:1S² 2S2 2P⁶ 3S² 3P¹
* Τάση να χάσετε ηλεκτρόνια: Λόγω των τριών ηλεκτρονίων σθένους, τόσο το βόριο όσο και το αλουμίνιο τείνουν να χάσουν αυτά τα ηλεκτρόνια για να επιτύχουν ένα σταθερό, πλήρες εξωτερικό κέλυφος, με αποτέλεσμα μια κατάσταση οξείδωσης +3. Αυτό τους καθιστά αντιδραστικά μέταλλα.
Ωστόσο, υπάρχουν επίσης κάποιες διαφορές:
* Ατομικό μέγεθος: Το αλουμίνιο είναι σημαντικά μεγαλύτερο από το βόριο επειδή έχει περισσότερα κελύφη ηλεκτρονίων.
* Μεταλλικός χαρακτήρας: Το αλουμίνιο είναι ένα πιο τυπικό μέταλλο από το βόριο. Το βόριο είναι ένα μεταλλοειδές, που σημαίνει ότι παρουσιάζει ιδιότητες τόσο των μετάλλων όσο και των μη μεταλλικών.
Συνοπτικά, Το βόριο και το αλουμίνιο μοιράζονται μια παρόμοια δομή ηλεκτρονίων λόγω της θέσης τους στον περιοδικό πίνακα, οδηγώντας σε ομοιότητες στη χημική τους συμπεριφορά, συγκεκριμένα την τάση τους να σχηματίζουν +3 ιόντα.