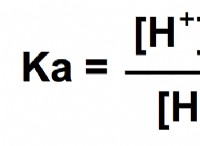Πώς επηρεάζει το οξύ ή η βάση το pH του αποσταγμένου νερού;
* Το αποσταγμένο νερό είναι ουδέτερο: Έχει ρΗ 7, που σημαίνει ότι έχει ισορροπία ιόντων υδρογόνου (Η+) και ιόντων υδροξειδίου (ΟΗ-).
* οξέα αυξάνουν τη συγκέντρωση ιόντων Η+: Όταν ένα οξύ προστίθεται σε απεσταγμένο νερό, απελευθερώνει ιόντα υδρογόνου (Η+) στο διάλυμα. Αυτό αυξάνει τη συγκέντρωση των ιόντων Η+, καθιστώντας τη λύση πιο όξινη. Η τιμή του ρΗ θα μειωθεί κάτω από 7.
* Οι βάσεις αυξάνουν τη συγκέντρωση των ουσών: Όταν μια βάση προστίθεται σε απεσταγμένο νερό, απελευθερώνει ιόντα υδροξειδίου (ΟΗ-) στο διάλυμα. Αυτό αυξάνει τη συγκέντρωση των ουσιών, καθιστώντας τη λύση πιο βασική. Η τιμή του ρΗ θα αυξηθεί πάνω από 7.
Εδώ είναι μια απλή αναλογία:
Σκεφτείτε μια κλίμακα όπου:
* αριστερή πλευρά: Πιο όξινο (χαμηλότερο pH)
* Δεξιά πλευρά: Πιο βασικό (υψηλότερο pH)
* Μέση: Ουδέτερο (ρΗ 7)
Η προσθήκη οξέος ωθεί την κλίμακα προς τα αριστερά, καθιστώντας το πιο όξινο. Η προσθήκη βάσης ωθεί την κλίμακα προς τα δεξιά, καθιστώντας την πιο βασική.
Σημαντική σημείωση:
* Τα ισχυρά οξέα και οι βάσεις έχουν μεγαλύτερο αντίκτυπο στο pH: Ισχυρά οξέα και βάσεις ιοντοποιούνται πλήρως στο νερό, απελευθερώνοντας μεγάλο αριθμό ιόντων Η+ ή ΟΗ, με αποτέλεσμα σημαντική αλλαγή του ρΗ.
* Τα αδύναμα οξέα και οι βάσεις έχουν μικρότερη επίδραση στο pH: Μόνο εν μέρει ιονίζουν στο νερό, απελευθερώνοντας λιγότερα Η+ ή ΟΗ-ιόντα, με αποτέλεσμα μια μικρότερη αλλαγή ρΗ.
Ενημερώστε με αν θέλετε περισσότερες λεπτομέρειες ή έχετε άλλες ερωτήσεις.