Ποιο είναι το πλεονέκτημα του προγραμματισμού θερμοκρασίας στην αέρια χρωματογραφία
Οι ρυθμίσεις του προφίλ θερμοκρασίας κατά τη διάρκεια της αέριας χρωματογραφίας αλλάζουν τον ρυθμό ράμπας των συστατικών του μείγματος, επιτρέποντας τη γρήγορη έκλουση του επιθυμητού συστατικού. Κατά τον διαχωρισμό ενός μείγματος με άγνωστα συστατικά με αέρια χρωματογραφία, χρησιμοποιείται ένα γενικό πρόγραμμα θερμοκρασίας για τη διερεύνηση της συμπεριφοράς κατακράτησης των συστατικών. Η αέρια χρωματογραφία είναι μια αναλυτική τεχνική διαχωρισμού που χρησιμοποιείται στον διαχωρισμό ενός μείγματος πτητικών ενώσεων. Αρκετοί παράγοντες όπως τα σημεία βρασμού, το μοριακό βάρος και η σχετική πολικότητα των συστατικών του μείγματος, το μήκος της στήλης και οι ποσότητες των υλικών που εγχέονται είναι υπεύθυνοι για τον διαχωρισμό του μείγματος.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η Αέρια Χρωματογραφία
– Ορισμός, Αρχή, Εφαρμογές
2. Ποιο είναι το πλεονέκτημα του προγραμματισμού θερμοκρασίας στην αέρια χρωματογραφία
– Επίδραση του προγραμματισμού θερμοκρασίας στον διαχωρισμό
Βασικοί όροι:Σημείο βρασμού, Ανιχνευτής, Αέρια Χρωματογραφία, Κινητή Φάση, Στατική Φάση

Τι είναι η Αέρια Χρωματογραφία
Η αέρια χρωματογραφία είναι μια μέθοδος διαχωρισμού για πτητικά συστατικά ενός μείγματος χρησιμοποιώντας τη διαφορική κατανομή μεταξύ μιας αέριας κινητής φάσης και μιας υγρής στατικής φάσης. Η κινητή φάση είναι ένα αδρανές αέριο όπως το αργό, το ήλιο ή το υδρογόνο. Η υγρή στατική φάση επικαλύπτει την εσωτερική πλευρά της στήλης ως ένα λεπτό στρώμα στην αέρια χρωματογραφία.
Τα πτητικά συστατικά κινούνται μέσω της στατικής φάσης μαζί με τη στατική φάση. Ο διαχωρισμός των μορίων μέσα σε ένα μείγμα εξαρτάται από διάφορους παράγοντες:
- Σημεία βρασμού των συστατικών στο μείγμα – Τα συστατικά με χαμηλά σημεία βρασμού εκλούονται γρήγορα.
- Μοριακό βάρος των συστατικών του μείγματος – Τα συστατικά με χαμηλότερο μοριακό βάρος εκλούονται γρήγορα.
- Σχετική πολικότητα των συστατικών σε σχέση με την πολικότητα της στατικής φάσης – Οι πολικές ενώσεις αλληλεπιδρούν περισσότερο με τη στατική φάση και εκλούονται αργά.
- Θερμοκρασία στήλης – Οι υψηλότερες θερμοκρασίες στήλης εκλούουν όλα τα στοιχεία πιο γρήγορα από τη στήλη.
- Μήκος στήλης – Τα μεγαλύτερα μήκη της στήλης αυξάνουν τον χρόνο έκλουσης. Όμως, δίνει έναν σωστό διαχωρισμό.
- Ποσότητες υλικών που εγχύονται – Οι υψηλότερες ποσότητες από ένα συγκεκριμένο συστατικό αυξάνουν τον χρόνο έκλουσης.
Τα όργανα της αέριας χρωματογραφίας παρουσιάζονται στο σχήμα 1 .
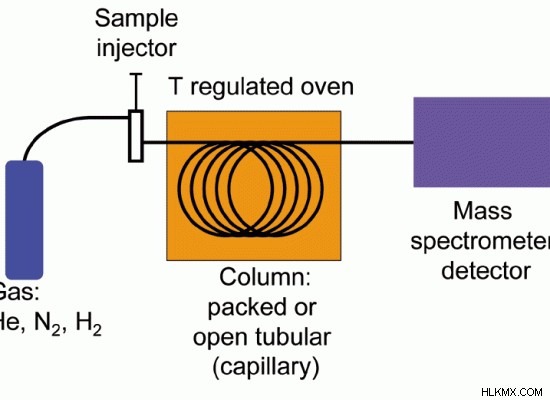
Εικόνα 1:Αέρια χρωματογραφία
Ένας ανιχνευτής χρησιμοποιείται για την αναγνώριση των διαχωρισμένων συστατικών του μείγματος σε σχέση με το χρόνο και παράγει ένα χρωματογράφημα. Κάθε κορυφή του χρωματογράμματος αντιπροσωπεύει έναν συγκεκριμένο τύπο συστατικού στο μείγμα. Σε ένα καθορισμένο σύνολο συνθηκών, ο χρόνος έκλουσης μιας συγκεκριμένης ένωσης είναι σταθερά. Ως εκ τούτου, οι ενώσεις του χρωματογράμματος μπορούν να αναγνωριστούν με βάση το χρόνο έκλουσης (ποιοτική μέτρηση). Το μέγεθος της κορυφής αντιπροσωπεύει την ποσότητα του συγκεκριμένου συστατικού (ποσοτική μέτρηση).
Ποιο είναι το πλεονέκτημα του προγραμματισμού θερμοκρασίας στην αέρια χρωματογραφία
Η αέρια χρωματογραφία χρησιμοποιεί δύο μεθόδους στον έλεγχο της θερμοκρασίας. ισοθερμική λειτουργία και προγραμματισμός θερμοκρασίας.
Ισοθερμική λειτουργία
Κατά τη διάρκεια της ισοθερμικής λειτουργίας, η στήλη λειτουργεί σε σταθερή θερμοκρασία καθ' όλη τη διάρκεια της διαδικασίας. Η θερμοκρασία στο μέσο του εύρους σημείου βρασμού χρησιμοποιείται ως ισοθερμική θερμοκρασία. Υπάρχουν μειονεκτήματα σε αυτή τη μέθοδο όταν το δείγμα περιέχει βαριές ενώσεις με υψηλότερα μοριακά βάρη και υψηλότερα σημεία βρασμού. Αυτά τα μειονεκτήματα περιλαμβάνουν:
- Κακή ανάλυση ελαφρύτερων εξαρτημάτων σε υψηλότερες θερμοκρασίες
- Ευρείς κορυφές για τις ενώσεις που εκλούονται αργότερα
- Φαινόμενο μεταφοράς των βαρύτερων εξαρτημάτων ή κορυφών φάντασμα λόγω αποσύνθεσης
- Μεγαλύτεροι χρόνοι λειτουργίας
- Χαμηλότερη απόδοση δείγματος
Προγραμματισμός θερμοκρασίας
Κατά τη λειτουργία προγραμματισμού θερμοκρασίας, η θερμοκρασία της στήλης αυξάνεται συνεχώς με κυρίαρχο ρυθμό. Ο ρυθμός ράμπας ή ο ρυθμός έκλουσης είναι ανάλογος με τη θερμοκρασία της στήλης. Στην αρχή, χρησιμοποιεί χαμηλότερες θερμοκρασίες που δίνουν μεγαλύτερη ανάλυση ελαφρύτερων ενώσεων. Με την αύξηση της θερμοκρασίας, ο ρυθμός ράμπας των βαρύτερων ενώσεων αυξάνεται επίσης. Αυτό δίνει πιο έντονες κορυφές για βαρύτερες ενώσεις. Τα πλεονεκτήματα του προγραμματισμού θερμοκρασίας παρατίθενται παρακάτω.
- Υψηλή ανάλυση ελαφρύτερων ενώσεων
- Αιχμηρές κορυφές για βαρύτερες ενώσεις
- Μειωμένοι χρόνοι εκτέλεσης
- Μικρότερη μεταφορά
- Μεγαλύτερη απόδοση δείγματος
- Εκτεταμένο εύρος εφαρμογής από μία στήλη
Συμπέρασμα
Η αέρια χρωματογραφία είναι μια αναλυτική μέθοδος διαχωρισμού πτητικών ενώσεων από ένα μείγμα. Διαχωρίζει τις ενώσεις κυρίως με βάση το σημείο βρασμού και το μοριακό βάρος. Ο προγραμματισμός θερμοκρασίας επιτρέπει την υψηλότερη ανάλυση ελαφρύτερων ενώσεων και αιχμηρές κορυφές για βαρύτερες ενώσεις, μειώνοντας τους μακροχρόνιους χρόνους που δημιουργούνται από βαρύτερες ενώσεις.
Αναφορά:
1. «Έλεγχος θερμοκρασίας της αέριας χρωματογραφικής στήλης». Lab-Training.com , 29 Δεκεμβρίου 2015, Διαθέσιμο εδώ.
Εικόνα Ευγενική προσφορά:
1. "Gcms schematic" Από K. Murray (Kkmurray) – Δική εργασία (CC BY-SA 3.0) μέσω Commons Wikimedia




