Γιατί το άζωτο είναι αέριο;
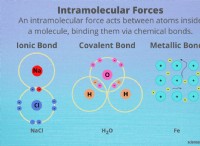
* Μοριακή δομή του αζώτου: Το άζωτο υπάρχει ως διατομικό μόριο (Ν2), που σημαίνει ότι δύο άτομα αζώτου συνδέονται μεταξύ τους. Αυτός ο ισχυρός τριπλός δεσμός μέσα στο μόριο το καθιστά πολύ σταθερό.
* Van der Waals Δυνάμεις: Οι μόνες διαμοριακές δυνάμεις που υπάρχουν μεταξύ των μορίων αζώτου είναι οι αδύναμες δυνάμεις van der Waals. Αυτές οι δυνάμεις προκύπτουν από προσωρινές διακυμάνσεις στην κατανομή ηλεκτρονίων γύρω από τα μόρια.
* Χαμηλό σημείο βρασμού: Οι αδύναμες δυνάμεις van der Waals ξεπερνούνται εύκολα με θερμική ενέργεια σε θερμοκρασία δωματίου. Αυτό σημαίνει ότι τα μόρια αζώτου έχουν αρκετή ενέργεια για να κινούνται ελεύθερα και ανεξάρτητα, με αποτέλεσμα μια αέρια κατάσταση. Το σημείο βρασμού του αζώτου είναι -196 ° C, το οποίο είναι πολύ χαμηλό σε σύγκριση με άλλα στοιχεία.
Σε αντίθεση:
* ισχυρότερες διαμοριακές δυνάμεις: Άλλα στοιχεία, όπως το οξυγόνο (Ο2) ή το νερό (H2O), έχουν ισχυρότερες ενδομοριακές δυνάμεις (όπως οι δεσμοί υδρογόνου στο νερό) που απαιτούν περισσότερη ενέργεια για να σπάσει, επιτρέποντάς τους να υπάρχουν σε υγρές ή στερεές καταστάσεις σε θερμοκρασία δωματίου.
Συνοπτικά: Οι αδύναμες διαμοριακές δυνάμεις του αζώτου και το χαμηλό σημείο βρασμού είναι οι κύριοι λόγοι για τους οποίους υπάρχει ως αέριο σε θερμοκρασία δωματίου.