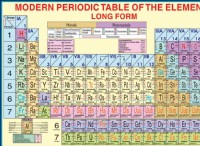
Τι είναι τα ενεργά μη μέταλλα;
Εδώ είναι γιατί:
* Τα μη-μετάλλια θεωρούνται γενικά λιγότερο αντιδραστικά από τα μέταλλα. Τείνουν να κερδίζουν ηλεκτρόνια για να σχηματίσουν αρνητικά ιόντα (ανιόντα).
* Η αντιδραστικότητα είναι σχετική. Ακόμη και μέσα στην ομάδα των μη μετάλλων, μερικοί είναι πιο αντιδραστικοί από άλλους. Για παράδειγμα, το φθοριοειδές είναι το πιο αντιδραστικό μη μέταλλο, ενώ το ήλιο είναι εξαιρετικά αντιδραστικό.
Αντί για "ενεργά μη μέταλλα", είναι πιο ακριβές να μιλήσουμε:
* Αντιδραστικά μη μέταλλα: Αυτά είναι μη μέταλλα που συμμετέχουν εύκολα σε χημικές αντιδράσεις. Παραδείγματα περιλαμβάνουν:
* αλογόνα (f, cl, br, i, at): Δημιουργούν εύκολα ενώσεις με μέταλλα και άλλα μη μέταλλα.
* οξυγόνο (o): Υποστηρίζει καύση και αντιδρά με πολλά στοιχεία για να σχηματίσουν οξείδια.
* Ανταγωνιστικά μη-μετάλλια: Αυτά τα μη μέταλλα είναι πολύ σταθερά και τείνουν να σχηματίζουν ενώσεις μόνο υπό συγκεκριμένες συνθήκες. Παραδείγματα περιλαμβάνουν:
* Noble Gases (He, Ne, Ar, Kr, Xe, RN): Έχουν ένα πλήρες εξωτερικό κέλυφος ηλεκτρονίων και είναι πολύ αντιδραστικά.
Είναι σημαντικό να θυμάστε: Οι όροι "ενεργοί" και "ανενεργοί" δεν είναι ακριβείς ταξινομήσεις στη χημεία. Η αντιδραστικότητα είναι ένα φάσμα και εξαρτάται από τις συγκεκριμένες συνθήκες και τους συνεργάτες αντίδρασης.