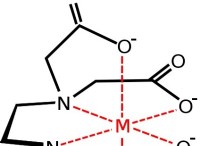
Τι είναι το ετεροτόμα;
Εδώ είναι μια κατανομή:
* Οργανική χημεία εστίαση: Ο όρος "ετεροατόμα" χρησιμοποιείται κυρίως στην οργανική χημεία, όπου ο άνθρακας και το υδρογόνο σχηματίζουν τη ραχοκοκαλιά των περισσότερων μορίων.
* ποικιλία στοιχείων: Τα ετεροατόματα μπορεί να είναι οποιοδήποτε στοιχείο από τον περιοδικό πίνακα εκτός από τον άνθρακα και το υδρογόνο. Τα κοινά παραδείγματα περιλαμβάνουν:
* οξυγόνο (o)
* αζώτου (n)
* θείο
* φωσφόρος (p)
* αλογόνα (f, cl, br, i)
* Αντίκτυπος στις μοριακές ιδιότητες: Η παρουσία ετεροατόμων επηρεάζει σημαντικά τη δομή, την αντιδραστικότητα και τις ιδιότητες των οργανικών μορίων. Εισάγουν:
* πολικότητα: Τα ετεροατόματα έχουν συχνά υψηλότερη ηλεκτροαρνητικότητα από τον άνθρακα και το υδρογόνο, οδηγώντας σε πολικούς δεσμούς και πολικά μόρια.
* Λειτουργικές ομάδες: Τα ετεροατόματα εμπλέκονται συχνά σε συγκεκριμένες λειτουργικές ομάδες (όπως οι αλκοόλες, οι αμίνες, οι κετόνες κ.λπ.), οι οποίες καθορίζουν τη χημική συμπεριφορά του μορίου.
* δεσμός υδρογόνου: Τα ετεροατόνια όπως το οξυγόνο και το άζωτο μπορούν να συμμετάσχουν στη δέσμευση υδρογόνου, επηρεάζοντας τις ιδιότητες όπως το σημείο βρασμού και τη διαλυτότητα.
Παραδείγματα:
* αιθανόλη (CH3CH2OH): Το άτομο οξυγόνου είναι ένα ετεροατόμα, καθιστώντας την αιθανόλη ένα πολικό μόριο και έναν καλό διαλύτη.
* μεθυλαμίνη (CH3NH2): Το άτομο αζώτου είναι ένα ετεροατόμα, δίνοντας μεθυλαμίνη τις βασικές του ιδιότητες.
* θειόλες (rsh): Το άτομο θείου είναι ένα ετεροατόμα, συμβάλλοντας στη χαρακτηριστική οσμή των θειολών.
Συνοπτικά: Τα ετεροατόματα είναι απαραίτητα στην οργανική χημεία καθώς εισάγουν ποικιλία και πολυπλοκότητα στα μόρια, οδηγώντας σε ένα ευρύ φάσμα ιδιοτήτων και λειτουργιών.