Ποια άτομα γενικά σχηματίζουν ομοιοπολικούς δεσμούς;
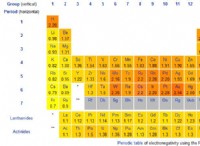
* Μη μετάλλια: Τα μη μέταλλα, όπως ο άνθρακας (C), το οξυγόνο (Ο), το άζωτο (Ν), το χλώριο (CL) και το θείο (S), συνήθως σχηματίζουν ομοιοπολικούς δεσμούς μεταξύ τους. Έχουν υψηλές τιμές ηλεκτροαρνητικότητας, που σημαίνει ότι προσελκύουν έντονα ηλεκτρόνια.
* Metalloids: Τα μεταλλοειδή, όπως το πυρίτιο (SI) και το γερμανικό (GE), μπορούν επίσης να σχηματίσουν ομοιοπολικούς δεσμούς, ειδικά με μη μέταλλα. Οι τιμές ηλεκτροαρνητικότητας τους πέφτουν μεταξύ εκείνων των μετάλλων και των μη μεταλλικών.
Γιατί μορφή ομοιοπολικών δεσμών:
* Όταν τα άτομα με παρόμοιο δεσμό τιμών ηλεκτροαρνητικότητας, ούτε το άτομο δεν έχει αρκετά ισχυρή έλξη για να αφαιρέσει πλήρως ένα ηλεκτρόνιο από το άλλο.
* Αντ 'αυτού, μοιράζονται ηλεκτρόνια για να επιτύχουν μια σταθερή διαμόρφωση ηλεκτρονίων, δημιουργώντας έναν ομοιοπολικό δεσμό.
Εξαιρέσεις:
Ενώ η πλειονότητα των ομοιοπολικών δεσμών εμφανίζεται μεταξύ των μη μεταλλικών, υπάρχουν κάποιες εξαιρέσεις:
* υδρογόνο (h): Το υδρογόνο μπορεί να σχηματίσει ομοιοπολικούς δεσμούς με μη μέταλλα και μερικά μέταλλα (όπως το λίθιο, το νάτριο και το κάλιο).
* Μερικοί δεσμοί μετάλλων-μετάλλων: Ορισμένα μέταλλα, ιδιαίτερα μεταβατικά μέταλλα, μπορούν να σχηματίσουν ομοιοπολικούς δεσμούς μεταξύ τους.
Key Takeaway: Οι ομοιοπολικοί δεσμοί είναι πιο συνηθισμένοι μεταξύ των ατόμων με παρόμοιες τιμές ηλεκτροαρνητικότητας, που εμφανίζονται κυρίως μεταξύ μη μεταλλικών και μεταλλοειδών.