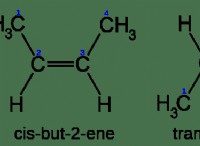
Όταν γράφετε τύπους θυμηθείτε ότι η ένωση είναι;
Ακολουθούν μερικά βασικά πράγματα που πρέπει να θυμάστε:
* Χημικά σύμβολα: Κάθε στοιχείο αντιπροσωπεύεται από ένα μοναδικό σύμβολο (π.χ. Η για υδρογόνο, Ο για οξυγόνο, ΝΑ για νάτριο).
* δείκτες: Αυτοί οι αριθμοί που γράφονται παρακάτω και στα δεξιά του συμβόλου του στοιχείου υποδεικνύουν πόσα άτομα αυτού του στοιχείου υπάρχουν στην ένωση. Για παράδειγμα, το H₂O έχει δύο άτομα υδρογόνου (Η) και ένα άτομο οξυγόνου (Ο).
* Ιωνικές ενώσεις: Αυτές οι ενώσεις σχηματίζονται μεταξύ μετάλλων και μη μέταλλων. Ο τύπος καθορίζεται με την εξισορρόπηση των χρεώσεων των εμπλεκομένων ιόντων. Για παράδειγμα, το χλωριούχο νάτριο (NaCl) σχηματίζεται από το συνδυασμό ιόντων νατρίου (Na+) και χλωριούχου ιόντων (Cl-).
* ομοιοπολικές ενώσεις: Αυτές οι ενώσεις σχηματίζονται μεταξύ μη μεταλλικών. Ο τύπος καθορίζεται από τον αριθμό των ηλεκτρονίων που μοιράζονται μεταξύ των ατόμων. Για παράδειγμα, το διοξείδιο του άνθρακα (CO₂) έχει ένα άτομο άνθρακα (C) και δύο άτομα οξυγόνου (O₂).
Συνοπτικά, ένας σύνθετος τύπος σας λέει ποια στοιχεία υπάρχουν και πόσα άτομα κάθε στοιχείου βρίσκονται σε ένα μόνο μόριο ή μονάδα της ένωσης.