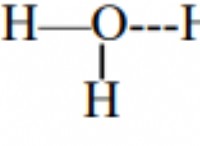Όταν τα μη μέταλλα αντιδρούν με άλλα άτομα να κάνουν τι ηλεκτρόνια;
Εδώ είναι γιατί:
* Τα μη μετάλλια έχουν υψηλή ηλεκτροαρνητικότητα: Αυτό σημαίνει ότι έχουν ισχυρή έλξη για τα ηλεκτρόνια.
* θέλουν να επιτύχουν μια σταθερή διαμόρφωση ηλεκτρονίων: Τα μη μέταλλα έχουν συνήθως ένα σχεδόν πλήρες εξωτερικό κέλυφος ηλεκτρονίων. Με την απόκτηση ηλεκτρονίων, μπορούν να ολοκληρώσουν αυτό το εξωτερικό κέλυφος και να γίνουν πιο σταθεροί.
Ας απεικονίσουμε με ένα παράδειγμα:
* οξυγόνο (o) είναι ένα μέταλλο με έξι ηλεκτρόνια στο εξωτερικό κέλυφος του. Χρειάζεται δύο ακόμη ηλεκτρόνια για να επιτευχθεί μια σταθερή διαμόρφωση όπως αυτή του Neon Nole Neon.
* Όταν το οξυγόνο αντιδρά με ένα μέταλλο σαν νάτριο (Na), τα κέρδη Δύο ηλεκτρόνια από άτομα νατρίου, σχηματίζοντας ιόν οξειδίου (o²⁻). Τα άτομα νατρίου, με τη σειρά τους, χάνουν ηλεκτρόνια και γίνονται θετικά φορτισμένα ιόντα νατρίου (Na⁺).
Αυτή η διαδικασία απόκρισης και απώλειας ηλεκτρονίων οδηγεί στο σχηματισμό ιοντικών δεσμών , όπου τα αντίθετα φορτισμένα ιόντα προσελκύουν ο ένας τον άλλον.