Τι είναι ένα μόριο που ονομάζεται που υφίσταται αντίδραση αποσύνθεσης αποδίδει προϊόντα ιόντων υδρογόνου και ανιόντων;
Εδώ είναι γιατί:
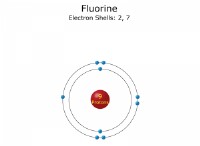
* οξέα είναι ουσίες που δίνουν ιόντα υδρογόνου (Η+) όταν διαλύονται σε νερό.
* αντίδραση αποσύνθεσης είναι μια αντίδραση όπου ένα μόνο αντιδραστήριο διασπάται σε δύο ή περισσότερα προϊόντα.
Παράδειγμα:
Η αποσύνθεση του υδροχλωρικού οξέος (HCl) στο νερό:
HCl (aq) → H + (aq) + cl- (aq)
* Το HCl είναι το οξύ.
* Η+ είναι το ιόν υδρογόνου.
* Cl- είναι το ανιόν (ιόν χλωριούχου).
Σημείωση: Η αντοχή ενός οξέος εξαρτάται από το πόσο εύκολα δωρίζει ιόντα υδρογόνου. Τα ισχυρά οξέα δίνουν εύκολα ιόντα Η+, ενώ τα αδύναμα οξέα δίνουν ιόντα Η+ λιγότερο εύκολα.