Θεωρητική μελέτη μη ομοιοπολικών αλληλεπιδράσεων σε βενζόλιο και υποκατεστημένο βενζόλιο

Ο ρόλος της μη ομοιοπολικής αλληλεπίδρασης σε διάφορες φυσικές, χημικές και βιοχημικές διεργασίες είναι ευρέως γνωστός και, ως εκ τούτου, έχουν προσελκύσει πολλούς ερευνητές στη φύση τους [1-5]. Αυτό έχει γίνει ένα από τα πρόσφατα και κύρια ενδιαφέροντα για την υπολογιστική χημεία να κατανοήσει και να χαρακτηρίσει ποικιλίες μη ομοιοπολικής αλληλεπίδρασης.
Μεταξύ αυτών των μη ομοιοπολικών αλληλεπιδράσεων, ο δεσμός υδρογόνου αναλύεται κυρίως λόγω του κρίσιμου ρόλου του στη σταθεροποίηση διαφόρων υπερμοριακών πλαισίων, στις αντιδράσεις μεταφοράς πρωτονίων, στην κρυσταλλική μηχανική και άλλα [6-9]. Ωστόσο, πρόσφατα μόρια υποκατεστημένα με αλογόνο (κυρίως φθορίου) βρέθηκε ότι αυξάνουν τον ρόλο άλλων τύπων αλληλεπίδρασης και γίνονται ένας διευρυνόμενος τομέας τόσο της πειραματικής όσο και της θεωρητικής έρευνας [10-13].
Ενώ η αλληλεπίδραση του βενζολίου με το νερό λαμβάνει χώρα μέσω του ατόμου υδρογόνου του νερού και του νέφους π του βενζολίου, η αλληλεπίδραση του νερού με το φθοριούχο βενζόλιο λαμβάνει χώρα μέσω του μοναδικού ζεύγους του ατόμου οξυγόνου του νερού και του π νέφους του βενζολίου του βενζολίου (Σχήμα 1). Αυτή η αλληλεπίδραση μοναχικού ζεύγους-π έχει πρόσφατα επαληθευτεί τόσο θεωρητικά όσο και πειραματικά [12]. Η πρώτη πειραματική απόδειξη της αλληλεπίδρασης μοναχικού ζεύγους-π δόθηκε από τον Reedijk και τους συνεργάτες του το 2004 στο σύμπλεγμα μεταξύ Cl και πυριδίνης [14]. Ο Meyer και οι συνεργάτες του [15] την ίδια χρονιά ανέφεραν πειραματικά στοιχεία για τη σταθεροποιητική αλληλεπίδραση μεταξύ Cl- και τριαζίνης, πυροδοτώντας περαιτέρω θεωρητικές και πειραματικές έρευνες σε αυτόν τον τομέα. Πρόσφατα, η περιστροφική φασματοσκοπία σε συνδυασμό με θεωρητικούς υπολογισμούς παρείχαν μια ξεκάθαρη απόδειξη της αλληλεπίδρασης μοναχικού ζεύγους-οπής π μεταξύ του ατόμου οξυγόνου του νερού και του νέφους π του φθοριούχου βενζολίου (Σχήμα 1b) [12,16].
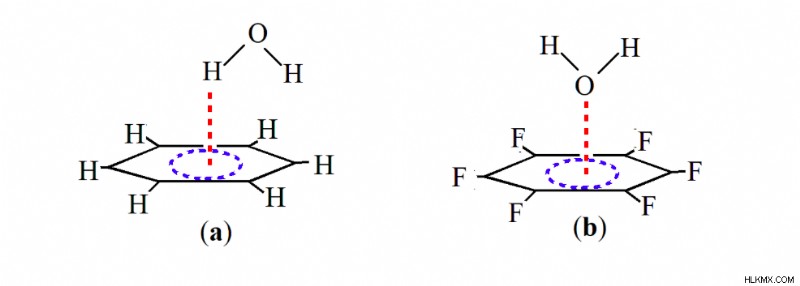
Ο σχηματισμός αυτής της αλληλεπίδρασης μοναχικού ζεύγους-π διευκολύνεται από την επαγωγική επίδραση των ατόμων φθορίου, η οποία αφαιρεί την πυκνότητα ηλεκτρονίων από τον δακτύλιο βενζολίου και δημιουργεί μια «οπή» στην περιοχή κάθετη στο μοριακό πλαίσιο. Αυτή η περιοχή αυτής της τρύπας μπορεί να προσελκύσει μεμονωμένα ζεύγη ατόμων οξυγόνου και οδηγεί στο σχηματισμό αυτής της αλληλεπίδρασης μοναχικού ζεύγους-π. Έτσι, φαίνεται ότι αυτή η αλληλεπίδραση μοναχικού ζεύγους-π είναι επίσης ανταγωνιστική με τους παραδοσιακούς δεσμούς υδρογόνου στη σταθεροποίηση πολλών υπερμοριακών πλαισίων. Εμπνευσμένοι από αυτό το εύρημα, πραγματοποιήσαμε μια λεπτομερή θεωρητική μελέτη σχετικά με τη δομή, την ενέργεια και την τοπολογία της πυκνότητας ηλεκτρονίων ορισμένων επιλεγμένων μορίων, όπως φαίνεται στο Σχήμα 2. Τα μόρια που εξετάζονται σε αυτή τη μελέτη είναι το βενζόλιο (Β), το εξαφθοροβενζόλιο (HFB) , εξακυανοβενζόλιο (HCB) και 1,3,5-τρινιτροβενζόλιο (TNB) και εξετάσαμε την αλληλεπίδρασή τους με το μοναχικό ζεύγος καθώς και με δότες δεσμών υδρογόνου όπως το H2 O, NH3 , HF και HCl.
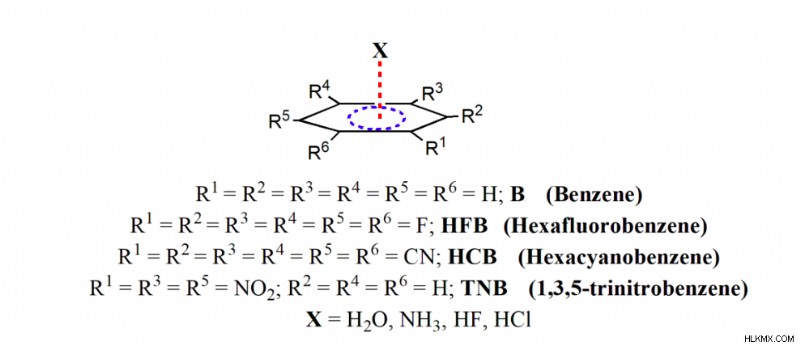
Η αλληλεπίδραση αυτών των μορίων με το βενζόλιο λαμβάνει χώρα μέσω των ατόμων Η του H2 O, NH3 , HF, HCl και το π νέφος του βενζολίου υπονοώντας ότι το π νέφος του βενζολίου δρα σαν ένας σωρός πυκνότητας ηλεκτρονίων που έλκει το ηλεκτροθετικό άτομο Η αυτών των μορίων. Από την άλλη πλευρά, η εισαγωγή υποκαταστατών απόσυρσης ηλεκτρονίων όπως F, CN, NO2 κ.λπ. στο βενζόλιο καθιστά την αρωματική επιφάνεια ελλειμματική ηλεκτρονίων που στη συνέχεια έλκει την περιοχή του μοναχικού ζεύγους του H2 O, NH3 , HF, μόρια HCl. Έτσι, η αρωματική επιφάνεια αυτών των υποκατεστημένων βενζολίων δρα σαν σωρό. Τόσο η ηλεκτροστατική όσο και η διασπορά, είναι οι κυρίαρχοι παράγοντες που συμβάλλουν στην ελκυστική αλληλεπίδραση. Η κυριαρχία των αλληλεπιδράσεων διασποράς δείχνει προς την ελεύθερη περιστροφή του H2 O, NH3 μόρια , HF και HCl, τα οποία είναι επίσης σύμφωνα με την πρόσφατη πειραματική παρατήρηση [12].
Αυτά τα ευρήματα περιγράφονται στο άρθρο με τίτλο Μη ομοιοπολική αλληλεπίδραση στο βενζόλιο και το υποκατεστημένο βενζόλιο:Μια θεωρητική μελέτη, που δημοσιεύτηκε πρόσφατα στο περιοδικό Computational and Theoretical Chemistry. Αυτή η εργασία διεξήχθη από τους Chayanika Kashyap, Sabnam S. Ullah, Lakhya J. Mazumder και Ankur Kanti Guha από το Cotton University.
Αναφορές:
- Μοριακές αλληλεπιδράσεις. Από το van der Waals μέχρι τα Strongly Bound Complexes. Εκδ. S. Scheiner, John Wiley &Sons, Chichester, 1997.
- H –J. Schneider, Angew. Chem. Int. Εκδ. , 48 (2009) 3924-3977.
- Σ. Hobza, K. Muller-Dethlefs, Μη ομοιοπολικές αλληλεπιδράσεις, θεωρία και πείραμα . Royal Society of Chemistry, Thomas Graham House, Science Park, Milton Road, Cambridge, Ηνωμένο Βασίλειο, 2010.
- Σ. Politzer, K. E. Riley, F. A. Bulat, J. S. Murray, Perspectives on halogen bonding and other σ-hole interactions:Lex parsimoniae (Occam’s Razor). Υπολογιστής. Θεωρ. Chem., 998 (2012) 2-8.
- S. J. Grabowski, Οι δεσμοί υδρογόνου και αλογόνου διέπονται από τους ίδιους μηχανισμούς. Phys. Chem. Chem. Phys. 15 (2013) 7249-7259 και αναφορές σε αυτό.
- Γ.Α. Jeffrey, Εισαγωγή στον δεσμό υδρογόνου , Oxford University Press, Νέα Υόρκη, 1997.
- S. Scheiner, Hydrogen Bonding, A Theoretical Perspective , Oxford University Press, Νέα Υόρκη, 1997.
- Μ. Nishio, M. Hirota, Y. Umezawa, The CH/ π Αλληλεπίδραση, Στοιχεία, Φύση και Συνέπειες , Wiley-VCH, Νέα Υόρκη, 1998.
- Δεσμός υδρογόνου – Νέες πληροφορίες , Εκδ. S.J. Grabowski, Vol. 3 της σειράς:Προκλήσεις και πρόοδοι στην Υπολογιστική Χημεία και τη Φυσική , Εκδ. J. Leszczynski, Springer, 2006.
- Μ. Cametti, B. Crousse, P. Metrangolo, R. Milani, G. Resnati, The fluorous effect in biomolecular applications. Chem. Soc. Αναθ. 41 (2012) 31- 42.
- R. Berger, G. Resnati, P. Metrangolo, E. Weber, J. Hulliger, Οργανικές ενώσεις φθορίου:μια εξαιρετική ευκαιρία για ενισχυμένες ιδιότητες υλικών. Chem. Soc. Αναθ. 40 (2011) 3496-3508.
- Λ. Evangelisti, K. Brendel, H. Mäder, W. Caminati, S. Melandri, Rotational spectroscopy probes water flipping by full fluorination of benzene. Angew. Chem. Int. Έκδ, 56 (2017) 13699-13703.
- Ν. Mohan, C. H. Suresh, A. Kumar, S. Gadre, Molecular electrostatics for probing lone pair–π Interactions. Phys. Chem. Chem. Phys. 15 (2013) 18401-18409 και αναφορές σε αυτό.
- Σ. De Hoog, P. Gamez, I. Mutikainen, U. Turpeinen, J. Reedijk, An Aromatic Anion Receptor:Anion–π Interactions do Exist. Angew. Chem., Int. Εκδ. 43 (2004) 5815-5817.
- S. Demeshko, S. Dechert, F. Meyer, Anion−π Interactions in a Carousel Copper(II)−Triazine Complex. Μαρμελάδα. Chem. Soc., 126 (2004) 4508-4509.
- Α. Bauzá, T. J. Mooibroek, A. Frontera, The Bright Future of Unconventional σ/π-Hole Interactions. ChemPhysChem. 16 (2015) 2496-2517.




