Γιατί η ζάχαρη εξαφανίζεται όταν διαλύεται στο νερό;
Όταν η ζάχαρη αναμιγνύεται με νερό, οι διαμοριακές δυνάμεις που συγκρατούν τη ζάχαρη είναι πιο αδύναμες από τις δυνάμεις των μορίων του νερού. Τα μόρια του νερού περιβάλλουν τη ζάχαρη και την απομακρύνουν μέσα στο διάλυμα. Η ανάδευση του μείγματος βοηθά στην ταχύτερη διάλυση της ζάχαρης φέρνοντας περισσότερα σωματίδια σε επαφή με το νερό.
Πρόσφατα βρέθηκα σε ένα παιδικό πάρτι γενεθλίων περιτριγυρισμένος από μια ντουζίνα παιδιά με απόλυτη έκρηξη (και ομολογουμένως, δυσκολεύοντας τους οικοδεσπότες). Έτυχε που ενώ έτρωγα τα μερίδια μου από μπισκότα, βρέθηκα δίπλα σε μερικά παιδιά που μιλούσαν για τη ζάχαρη που είχε προστεθεί στον χυμό τους. Αναρωτιόντουσαν πού είχε πάει, γιατί φαινόταν να εξαφανίζεται ως δια μαγείας μετά την ανάδευση.
Ήθελα να τους πω ότι η ζάχαρη εξαφανίστηκε γιατί διαλύθηκε. Προφανώς, όλοι γνωρίζουμε ότι όταν η ζάχαρη αναμιγνύεται με νερό, εξαφανίζεται γρήγορα αφού ανακατέψετε το υγρό για μια ή δύο στιγμές. Η ερώτηση δεν μπορεί να απαντηθεί πλήρως λέγοντας απλώς «επειδή διαλύεται», μαζί με ένα γούρλισμα του ματιού και ένα ανασήκωμα των ώμων.
Λοιπόν, ας πάμε στο κάτω μέρος αυτού. Πού στη Γη πηγαίνει η ζάχαρη μετά τη διάλυση;
Δυνάμεις που συγκρατούν τα συστατικά σωματίδια μαζί
Η φυσική κατάσταση (ή φάση) οποιασδήποτε ύλης καθορίζεται από τις δυνάμεις που συγκρατούν τα σωματίδια που την αποτελούν μαζί, δηλαδή τις διαμοριακές της δυνάμεις. Πάρτε τα στερεά, για παράδειγμα. Τα συστατικά μόρια που αποτελούν τα στερεά συγκρατούνται μεταξύ τους με ισχυρές διαμοριακές δυνάμεις σε μια άκαμπτη δομή (πλέγμα). Αυτό προσδίδει μια σειρά από φυσικές ιδιότητες στα στερεά, όπως αντοχή, ακαμψία, ασυμπίεση και άλλες.
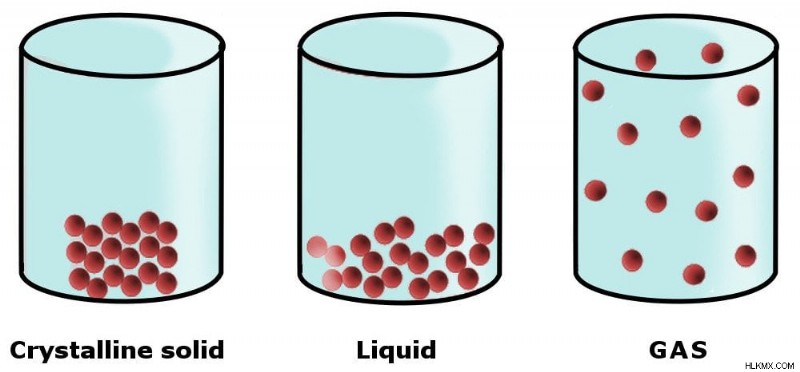
Διάταξη των συστατικών σωματιδίων σε στερεό, υγρό και αέριο
Στα υγρά, οι διαμοριακές δυνάμεις είναι πιο αδύναμες από τα στερεά, γι' αυτό και τα υγρά δεν έχουν ένα συγκεκριμένο σχήμα. Αντίθετα, παίρνουν το σχήμα του δοχείου στο οποίο φυλάσσονται.
Όντας ένα στερεό (και επομένως έχοντας μια δομή πλέγματος), το σχήμα και η εμφάνιση ενός κύβου ζάχαρης αποδίδονται στις ισχυρές ελκτικές δυνάμεις που συγκρατούν τα συστατικά του σωματίδια μαζί. Ωστόσο, όταν ο κύβος έρχεται σε επαφή με το νερό, αυτές οι δυνάμεις αναμιγνύονται και ο κύβος χάνει το σχήμα του, αποσυντίθεται γρήγορα.
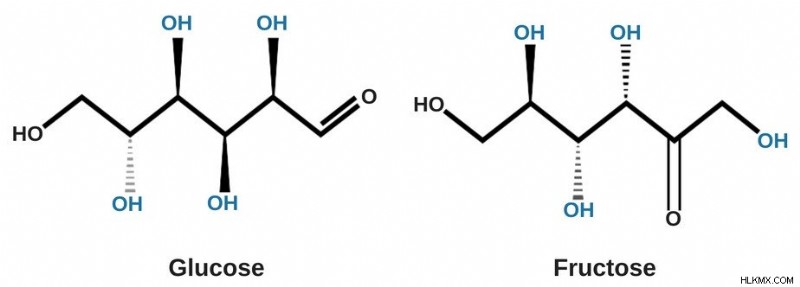
Βλέπετε, ένα μόριο σακχάρου αποτελείται από ομάδες υδροξυλίου (ΟΗ) που δημιουργούν εύκολα δεσμούς υδρογόνου με τα μόρια του νερού που τις περιβάλλουν. Τώρα, ένα πράγμα που πρέπει να γνωρίζετε για τους δεσμούς υδρογόνου είναι ότι είναι πολύ ισχυροί.
Στην πραγματικότητα, είναι μια από τις ισχυρότερες διαμοριακές έλξεις στη φύση, μόνο πιο αδύναμες από τους ιοντικούς και ομοιοπολικούς δεσμούς. Αυτοί οι δεσμοί είναι επίσης ισχυρότεροι από τις διαμοριακές δυνάμεις που συγκρατούν τα μόρια στο δικτυωτό σχήμα του κύβου. Ως αποτέλεσμα, τα μόρια του νερού περιβάλλουν τους μικροσκοπικούς κύβους ζάχαρης, τους απελευθερώνουν από τις ελκτικές δυνάμεις των γύρω μορίων και τους τραβούν μέσα στο διάλυμα. Αυτή η διαδικασία συνεχίζεται για λίγο (ανάλογα με ορισμένους παράγοντες, όπως η θερμοκρασία του νερού, ο κορεσμός, η ανάδευση κ.λπ.) μέχρι να διαχυθούν οι κύβοι και τελικά να εξαφανιστούν μετά τον πλήρη διαχωρισμό από την κύρια δομή.
Γιατί το ανακάτεμα βοηθά στην ταχύτερη διάλυση της ζάχαρης στο νερό;
Εάν ρίξετε απλώς ένα κομμάτι ζάχαρης σε ένα ποτήρι γεμάτο με νερό, η διάλυση θα είναι σημαντικά πιο αργή, καθώς τα μόρια του νερού μπορούν να έρθουν σε επαφή μόνο με τα σωματίδια στην επιφάνεια. Ωστόσο, όταν αναδεύετε ένα διάλυμα, ουσιαστικά φέρνετε περισσότερα σωματίδια σε επαφή με το νερό, κάνοντας τη διαδικασία διάλυσης σημαντικά πιο γρήγορη.
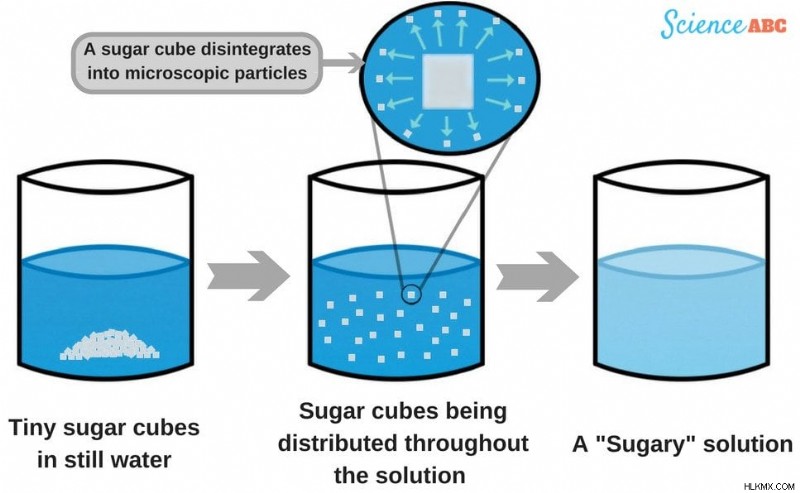
Οι κύβοι ζάχαρης διασπώνται σε μικροσκοπικά σωματίδια και αναμιγνύονται σε όλο το διάλυμα για να γίνουν τελικά αόρατοι με γυμνό μάτι
Ένα άλλο ερώτημα που μπερδεύει πολλούς είναι αν η διάλυση της ζάχαρης είναι φυσική ή χημική αλλαγή. Σημειώστε ότι είναι μια φυσική αλλαγή, γιατί για να είναι μια χημική αλλαγή, θα πρέπει να παραχθεί κάτι νέο ως αποτέλεσμα της διάλυσης. Παρεμπιπτόντως, αυτό δεν συμβαίνει. Το μόνο που λαμβάνετε μετά τη διάλυση της ζάχαρης στο νερό είναι ένα «ζαχαρούχο» διάλυμα, ούτε περισσότερο ούτε λιγότερο. Η ταυτότητα των συστατικών παραμένει αμετάβλητη.
Την επόμενη φορά που θα συναντήσετε ένα περίεργο παιδί που θα ρωτήσει για τους κύβους ζάχαρης που εξαφανίζονται όταν ανακατεύονται, αυτές οι πληροφορίες θα μπορούσαν να σας φανούν αρκετά χρήσιμες. Κυρίως, θυμηθείτε να μην ολοκληρώνετε τη συζήτηση λέγοντας απλώς «η ζάχαρη διαλύεται στο νερό».




