Τι είναι η σιλικόνη;
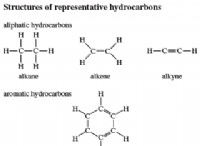
Σιλικόνες είναι ένας τύπος συνθετικού πολυμερούς, ένα υλικό κατασκευασμένο από μικρότερες, επαναλαμβανόμενες χημικές μονάδες που ονομάζονται μονομερή που συνδέονται μεταξύ τους σε μακριές αλυσίδες. Η σιλικόνη αποτελείται από μια ραχοκοκαλιά πυριτίου-οξυγόνου, με «πλευρικές αλυσίδες» που αποτελούνται από ομάδες υδρογόνου και/ή υδρογονάνθρακα που συνδέονται με τα άτομα πυριτίου. Επειδή η ραχοκοκαλιά της δεν περιέχει άνθρακα, η σιλικόνη θεωρείται ανόργανο πολυμερές , που διαφέρει από τα πολλάβιολογικά πολυμερή των οποίων η ραχοκοκαλιά είναι κατασκευασμένη από άνθρακα.
Οι δεσμοί πυριτίου-οξυγόνου στη ραχοκοκαλιά σιλικόνης είναι πολύ σταθεροί, δεσμεύονται μεταξύ τους πιο ισχυρά από τους δεσμούς άνθρακα-άνθρακα που υπάρχουν σε πολλά άλλα πολυμερή. Έτσι, η σιλικόνη τείνει να είναι πιο ανθεκτική στη θερμότητα από τα συμβατικά, οργανικά πολυμερή.
Οι πλευρικές αλυσίδες της σιλικόνης καθιστούν το πολυμερές υδρόφοβο, καθιστώντας το χρήσιμο για εφαρμογές που μπορεί να απαιτούν απώθηση νερού. Οι πλευρικές αλυσίδες, οι οποίες συνήθως αποτελούνται από ομάδες μεθυλίου, δυσκολεύουν επίσης την αντίδραση της σιλικόνης με άλλες χημικές ουσίες και την εμποδίζουν να κολλήσει σε πολλές επιφάνειες. Αυτές οι ιδιότητες μπορούν να ρυθμιστούν αλλάζοντας τις χημικές ομάδες που συνδέονται με τη ραχοκοκαλιά πυριτίου-οξυγόνου.
Η σιλικόνη στην καθημερινή ζωή
Η σιλικόνη είναι ανθεκτική, εύκολη στην κατασκευή και σταθερή σε ένα ευρύ φάσμα χημικών ουσιών και θερμοκρασιών. Για αυτούς τους λόγους, η σιλικόνη έχει εμπορευματοποιηθεί σε μεγάλο βαθμό και χρησιμοποιείται σε πολλές βιομηχανίες, όπως η αυτοκινητοβιομηχανία, οι κατασκευές, η ενέργεια, τα ηλεκτρονικά, τα χημικά, οι επικαλύψεις, τα υφάσματα και η προσωπική φροντίδα. Το πολυμερές έχει επίσης μια ποικιλία άλλων εφαρμογών, που κυμαίνονται από πρόσθετα έως μελάνια εκτύπωσης έως τα συστατικά που βρέθηκαν αποσμητικά.
Ανακάλυψη σιλικόνης
Ο χημικός Frederic Kipping επινόησε για πρώτη φορά τον όρο «σιλικόνη» για να περιγράψει τις ενώσεις που κατασκεύαζε και μελετούσε στο εργαστήριό του. Σκέφτηκε ότι θα έπρεπε να μπορεί να κάνει ενώσεις παρόμοιες με αυτές που θα μπορούσαν να παρασκευαστούν με άνθρακα και υδρογόνο, καθώς το πυρίτιο και ο άνθρακας μοιράζονται πολλές ομοιότητες. Το επίσημο όνομα για την περιγραφή αυτών των ενώσεων ήταν "σιλικοκετόνη", το οποίο συντόμευσε σε σιλικόνη.
Ο Kipping ενδιαφερόταν πολύ περισσότερο για τη συσσώρευση παρατηρήσεων σχετικά με αυτές τις ενώσεις παρά για να καταλάβει πώς ακριβώς λειτουργούσαν. Πέρασε πολλά χρόνια για να τα προετοιμάσει και να τα ονομάσει. Άλλοι επιστήμονες θα βοηθούσαν στην ανακάλυψη των θεμελιωδών μηχανισμών πίσω από τις σιλικόνες.
Στη δεκαετία του 1930, ένας επιστήμονας από την εταιρεία Corning Glass Works προσπαθούσε να βρει ένα κατάλληλο υλικό για να συμπεριλάβει στη μόνωση για ηλεκτρικά μέρη. Η σιλικόνη λειτούργησε για την εφαρμογή λόγω της ικανότητάς της να στερεοποιείται υπό τη θερμότητα. Αυτή η πρώτη εμπορική ανάπτυξη οδήγησε τη σιλικόνη στην ευρεία κατασκευή.
Σιλικόνη έναντι πυριτίου έναντι πυριτίου
Αν και οι λέξεις "σιλικόνη" και "πυρίτιο" γράφονται παρόμοια, δεν είναι το ίδιο.
Σιλικόνη περιέχει πυρίτιο, ένα ατομικό στοιχείο με ατομικό αριθμό 14. Το πυρίτιο είναι ένα φυσικό στοιχείο με πολλές χρήσεις, κυρίως ως ημιαγωγός στα ηλεκτρονικά. Η σιλικόνη, από την άλλη, είναι ανθρωπογενής και δεν μεταφέρει ηλεκτρισμό, καθώς είναι μονωτής. Η σιλικόνη δεν μπορεί να χρησιμοποιηθεί ως μέρος ενός τσιπ μέσα σε ένα κινητό τηλέφωνο, αν και είναι ένα δημοφιλές υλικό για θήκες κινητών τηλεφώνων.
Το "πυρίτιο", που ακούγεται σαν "πυρίτιο", αναφέρεται σε ένα μόριο που αποτελείται από ένα άτομο πυριτίου ενωμένο με δύο άτομα οξυγόνου. Ο χαλαζίας είναι κατασκευασμένος από πυρίτιο.
Τύποι σιλικόνης και οι χρήσεις τους
Υπάρχουν πολλές διαφορετικές μορφές σιλικόνης, οι οποίες διαφέρουν ως προς τον βαθμό διασταύρωσης . Ο βαθμός σταυροσύνδεσης περιγράφει πόσο διασυνδεδεμένες είναι οι αλυσίδες σιλικόνης, με υψηλότερες τιμές που καταλήγουν σε ένα πιο άκαμπτο υλικό σιλικόνης. Αυτή η μεταβλητή αλλάζει ιδιότητες όπως η αντοχή του πολυμερούς και το σημείο τήξης του.
Οι μορφές σιλικόνης, καθώς και ορισμένες από τις εφαρμογές τους, περιλαμβάνουν:
- Υγρά σιλικόνης , που ονομάζονται επίσης λάδια σιλικόνης, αποτελούνται από ευθείες αλυσίδες του πολυμερούς σιλικόνης χωρίς σταυροδεσμούς. Αυτά τα υγρά έχουν χρησιμοποιηθεί ως λιπαντικά, πρόσθετα βαφής και συστατικά σε καλλυντικά.
- τζελ σιλικόνης έχουν λίγες σταυροδεσμούς μεταξύ των πολυμερών αλυσίδων. Αυτά τα τζελ έχουν χρησιμοποιηθεί σε καλλυντικά και ως τοπική σύνθεση για τον ουλώδη ιστό, καθώς η σιλικόνη σχηματίζει ένα φράγμα που βοηθά το δέρμα να παραμείνει ενυδατωμένο. Τα τζελ σιλικόνης χρησιμοποιούνται επίσης ως υλικά για εμφυτεύματα στήθους και για το μαλακό μέρος ορισμένων πάτους παπουτσιών.
- Ελαστομερή σιλικόνης , που ονομάζονται επίσης λάστιχα σιλικόνης, περιλαμβάνουν ακόμη περισσότερους σταυροδεσμούς, δίνοντας ένα υλικό που μοιάζει με καουτσούκ. Αυτά τα λάστιχα έχουν βρει χρήση ως μονωτές στη βιομηχανία ηλεκτρονικών, σφραγίδες σε αεροδιαστημικά οχήματα και γάντια φούρνου για ψήσιμο.
- Ρητίνες σιλικόνης είναι μια άκαμπτη μορφή σιλικόνης και με υψηλή πυκνότητα σταυροδεσμών. Αυτές οι ρητίνες έχουν βρει χρήση σε ανθεκτικές στη θερμότητα επιστρώσεις και ως ανθεκτικά στις καιρικές συνθήκες υλικά για την προστασία των κτιρίων.
Τοξικότητα σιλικόνης
Επειδή η σιλικόνη είναι χημικά αδρανής και πιο σταθερή από άλλα πολυμερή, δεν αναμένεται να αντιδράσει με μέρη του σώματος. Ωστόσο, η τοξικότητα εξαρτάται από παράγοντες όπως ο χρόνος έκθεσης, η χημική σύνθεση, τα επίπεδα δόσης, ο τύπος έκθεσης, η απορρόφηση της χημικής ουσίας και η μεμονωμένη απόκριση.
Οι ερευνητές εξέτασαν την πιθανή τοξικότητα της σιλικόνης αναζητώντας επιδράσεις όπως ερεθισμός του δέρματος, αλλαγές στο αναπαραγωγικό σύστημα και μεταλλάξεις. Παρόλο που ορισμένοι τύποι σιλικόνης έδειξαν ότι μπορεί να ερεθίσουν το ανθρώπινο δέρμα, μελέτες έχουν δείξει ότι η έκθεση σε τυπικές ποσότητες σιλικόνης παράγει συνήθως λίγες έως καθόλου ανεπιθύμητες ενέργειες.
Βασικά σημεία
- Η σιλικόνη είναι ένας τύπος συνθετικού πολυμερούς. Έχει μια ραχοκοκαλιά πυριτίου-οξυγόνου, με "πλευρικές αλυσίδες" που αποτελούνται από ομάδες υδρογόνου ή/και υδρογονάνθρακα που συνδέονται με τα άτομα πυριτίου.
- Η ραχοκοκαλιά πυριτίου-οξυγόνου καθιστά τη σιλικόνη πιο σταθερή από τα πολυμερή που έχουν ραχοκοκαλιά άνθρακα-άνθρακα.
- Η σιλικόνη είναι ανθεκτική, σταθερή και εύκολη στην κατασκευή. Για αυτούς τους λόγους, έχει κυκλοφορήσει ευρέως στο εμπόριο και βρίσκεται σε πολλά είδη καθημερινής χρήσης.
- Η σιλικόνη περιέχει πυρίτιο, το οποίο είναι ένα χημικό στοιχείο που απαντάται στη φύση.
- Οι ιδιότητες της σιλικόνης αλλάζουν καθώς αυξάνεται ο βαθμός διασταύρωσης. Τα υγρά σιλικόνης, τα οποία δεν έχουν σταυροσύνδεση, είναι τα λιγότερο άκαμπτα. Οι ρητίνες σιλικόνης, οι οποίες έχουν υψηλό επίπεδο σταυροσύνδεσης, είναι οι πιο άκαμπτες.
Πηγές
Freeman, G. G. "Οι ευέλικτες σιλικόνες." The New Scientist , 1958.
Νέοι τύποι ρητίνης σιλικόνης ανοίγουν ευρύτερα πεδία εφαρμογής, Marco Heuer, Βιομηχανία χρωμάτων και επιστρώσεων.
"Τοξικολογία σιλικόνης." Στο Ασφάλεια εμφυτευμάτων στήθους σιλικόνης , εκδ. Bondurant, S., Ernster, V., and Herdman, R. National Academies Press, 1999.
"Σιλικόνες." The Essential Chemistry Industry.
Shukla, B., and Kulkarni, R. "Πολυμερή σιλικόνης:ιστορία και χημεία."
"The Technic εξερευνά τις σιλικόνες." The Michigan Technic , τόμ. 63-64, 1945, σσ. 17.
Wacker. Σιλικόνες:Ενώσεις και ιδιότητες.