Οξείδιο του μαγγανίου:Χημικός τύπος, ιδιότητες και χρήσεις
Το οξείδιο του μαγγανίου είναι η ανόργανη ένωση με τον χημικό τύπο MnO. Είναι ένα μαύρο-καφέ στερεό που εμφανίζεται φυσικά ως ορυκτό πυρολουσίτη. Το οξείδιο του μαγγανίου χρησιμοποιείται ως καταλύτης στην παραγωγή αλλυλικής αλκοόλης, χρωμάτων, έγχρωμου γυαλιού και κεραμικών. Είναι επίσης συστατικό λιπασμάτων και προσθέτων τροφίμων.
Ο όρος «οξείδιο του μαγγανίου» χρησιμοποιείται για να αναφέρεται σε οποιοδήποτε από τα διάφορα είδη οξειδίων του μαγγανίου που υπάρχουν στη φύση. Επιπλέον, το «οξείδιο του μαγγανίου» μπορεί επίσης να αναφέρεται σε ορισμένα ορυκτά μαγγανίου, όπως ο χαουσμαννίτης, ο μπιρνεσίτης, ο μαγγανοσίτης, ο μαγγανίτης κ.λπ.
Μαγγάνιο
Το μαγγάνιο (σύμβολο «Mn») είναι το 10ο πιο άφθονο από όλα τα στοιχεία που βρίσκονται φυσικά στον φλοιό της Γης. Είναι δεύτερο μόνο μετά τον σίδηρο ως το πιο κοινό φυσικό βαρύ μέταλλο στον πλανήτη. Βρίσκεται σε τεράστιες ποσότητες σε τήγματα και εναποθέσεις (όπως οι πηγματίτες).
Το μαγγάνιο εξαντλείται από μεταμορφωμένα και πυριγενή πετρώματα λόγω αλληλεπίδρασης με υπόγεια και επιφανειακά ύδατα. Μια άλλη ενδιαφέρουσα ποιότητα του μαγγανίου είναι ότι οξειδώνεται εύκολα, γεγονός που το κάνει να παράγει περισσότερα από τριάντα γνωστά οξείδιο του μαγγανίου ή ορυκτά υδροξειδίου.
Τι είναι το οξείδιο του μαγγανίου;
Ο όρος «οξείδιο μαγγανίου» μπορεί να χρησιμοποιηθεί για να αναφέρεται σε οποιοδήποτε από τα οξείδια και υδροξείδια του μαγγανίου, τα οποία περιλαμβάνουν, οξείδιο μαγγανίου (II) (ονομάζεται επίσης «βαθμού φερρίτη»), οξείδιο μαγγανίου (II, III), οξείδιο μαγγανίου (III) κ.λπ.
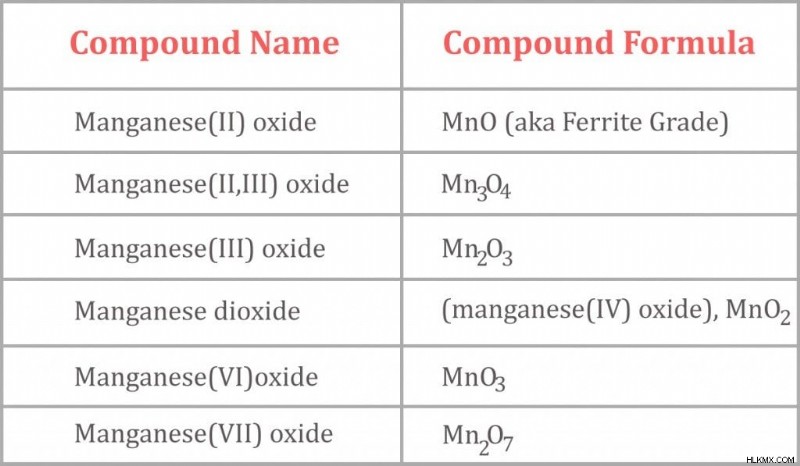
Μερικές από τις ενώσεις που είναι μεμονωμένα γνωστές ως «οξείδιο του μαγγανίου».
Υπάρχουν επίσης πολλά ορυκτά που αναφέρονται περιστασιακά ως οξείδια του μαγγανίου, όπως ο μαγγανοσίτης, ο μπιρνεσίτης και ο μαγγανίτης, για να αναφέρουμε μόνο μερικά.
Είναι προφανές ότι υπάρχουν περισσότερα από ένα «οξείδια μαγγανίου» εκεί έξω, αλλά αυτά που συνδέονται πιο συχνά με αυτό το όνομα είναι το οξείδιο του μαγγανίου (II) (MnO2) και το διοξείδιο του μαγγανίου (MnO).
Οξείδιο μαγγανίου (II)
Το οξείδιο του μαγγανίου (II) είναι στην πραγματικότητα μια ανόργανη ένωση και έχει τον χημικό τύπο MnO. Όπως πολλά άλλα μονοξείδια, έχει δομή αλατιού, που σημαίνει ότι τόσο τα κατιόντα όσο και τα ανιόντα είναι οκταεδρικά συντονισμένα. Αυτή η παρακάτω εικόνα θα σας βοηθήσει να οπτικοποιήσετε τη δομή του οξειδίου του μαγγανίου.
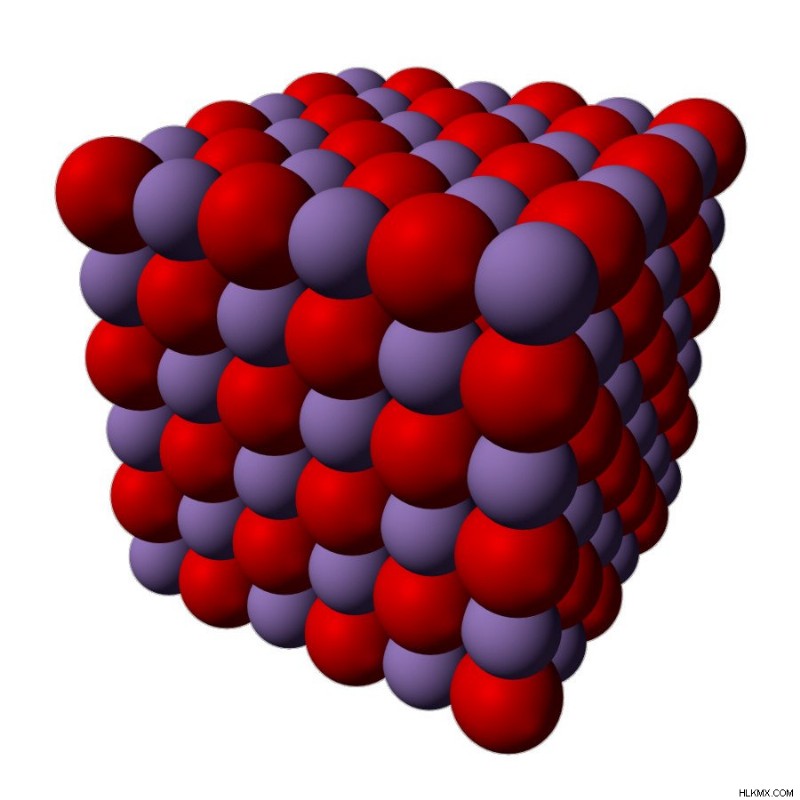
Οξείδιο μαγγανίου (II) (Πιστωτική φωτογραφία :CCoil / Wikimedia Commons)
Κατά τη διάρκεια χημικών αντιδράσεων, τα οξείδια του μαγγανίου (II) συμπεριφέρονται σαν ένα τυπικό ιοντικό οξείδιο. Ως εκ τούτου, όταν αλληλεπιδρά με ένα οξύ, μετατρέπεται στο αντίστοιχο άλας μαγγανίου και νερό.
Χρησιμοποιήσεις
Το οξείδιο του μαγγανίου είναι ένα πολύ γνωστό συστατικό των λιπασμάτων και των προσθέτων τροφίμων. Λόγω της αποτελεσματικότητάς του μόνο στη βιομηχανία λιπασμάτων, η ετήσια κατανάλωσή του κυμαίνεται σε χιλιάδες τόνους. Επιπλέον, το οξείδιο του μαγγανίου (II) χρησιμοποιείται ως καταλύτης στην παραγωγή αλλυλικής αλκοόλης, χρωμάτων, έγχρωμου γυαλιού, κεραμικών κ.λπ.
Οξείδιο μαγγανίου (IV) ή διοξείδιο μαγγανίου
Το οξείδιο του μαγγανίου (IV) είναι μια ανόργανη ένωση. Ο χημικός τύπος του είναι MnO2 και εμφανίζεται φυσικά ως ορυκτό πυρολουσίτης, που τυχαίνει να είναι συστατικό των οζιδίων μαγγανίου.

Οξείδιο του μαγγανίου (IV). (Φωτογραφία:Walkerma / Wikimedia Commons)
Οι περισσότεροι άνθρωποι συνδέουν το οξείδιο του μαγγανίου με το μαύρο εσωτερικό μιας μπαταρίας ξηρών κυψελών. Ωστόσο, είναι ενδιαφέρον να σημειωθεί ότι το οξείδιο εμφανίζεται σε μια μεγάλη ποικιλία άλλων τόπων και γεωλογικών πλαισίων:βρίσκεται σε εδάφη και ιζήματα, όπου υπάρχει ως λεπτόκοκκα αδρανή, καθώς και σε γλυκά και θαλάσσια οζίδια και σκυρόδεμα.
Ωστόσο, η πιο άφθονη εναπόθεση οξειδίων του μαγγανίου εμφανίζεται στους ωκεανούς ως οζίδια. Οζίδια μαγγανίου βρίσκονται σχεδόν σε όλα τα βάθη σε κάθε ωκεανό και θάλασσα του κόσμου. Απλώς για να σας δώσουμε κάποια εκτίμηση της πανταχού παρουσίας των μονάδων Mn, έχει υπολογιστεί ότι τα οζίδια μαγγανίου καλύπτουν περίπου το 10-30% του βαθέως δαπέδου του Ειρηνικού!
Χρησιμοποιήσεις
Η κύρια και πιο κοινή εφαρμογή του οξειδίου του μαγγανίου παρατηρείται σε μπαταρίες ξηρής κυψέλης (μπαταρίες ψευδαργύρου-άνθρακα ή κυψέλη d Leclanché). Οι μπαταρίες αντιπροσωπεύουν σημαντικό μέρος της συνολικής ετήσιας κατανάλωσης οξειδίου του μαγγανίου. Τα τελευταία χρόνια, ωστόσο, οι αλκαλικές μπαταρίες, οι οποίες χρησιμοποιούν επίσης οξείδιο του μαγγανίου, έχουν αρχίσει να κυριαρχούν στην αγορά.
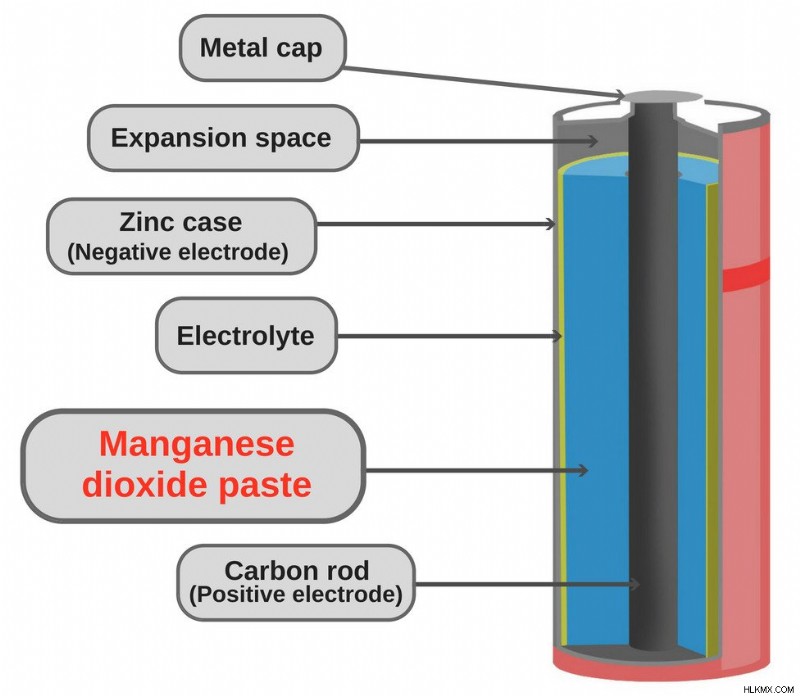
Έτσι φαίνεται μια μπαταρία ξηρής κυψέλης από μέσα.
Επιπλέον, χρησιμοποιείται ως πρόσθετο για ζωοτροφές, χρωστική για τούβλα, φυτικά λιπάσματα κ.λπ.
Ένα σημαντικό πράγμα που πρέπει να σημειωθεί σχετικά με το οξείδιο του μαγγανίου είναι ότι όταν έρχεται σε επαφή με τον αέρα και μολυνθεί, τα σωματίδια του μπορεί να προκαλέσουν δηλητηρίαση από μαγγάνιο ή μαγγανισμό , που μπορεί να οδηγήσει σε μια σειρά από ψυχιατρικές και κινητικές διαταραχές.