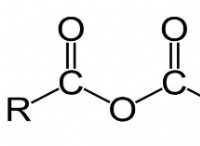
Μεσομερική επίδραση στη φαινόλη
Η έννοια του μεσομερικού φαινομένου, του μεσομερισμού και των Μεσομερών θεσπίστηκε από τον επιστήμονα Ingold το έτος 1938.
Προφανώς, το Mesomer είναι μια χροιά της λέξης resonance της οποίας η ιδέα δόθηκε από τον επιστήμονα Pauling. Είναι η ιδιότητα που κατέχουν οι λειτουργικές ομάδες σε μια χημική ένωση.
Το μεσομερικό φαινόμενο είναι το φαινόμενο στο οποίο ένα μόριο μπορεί να υπάρχει σε περισσότερες από μία δομές, αλλά καμία από τις οι δομές είναι θεμελιώδεις δομές.
Τι είναι το μεσομερικό φαινόμενο;
Η πολικότητα που αναπτύχθηκε μεταξύ των ατόμων ενός συζευγμένου συστήματος από τη μεταφορά ηλεκτρονίων ή τη μεταφορά ηλεκτρονίων pi–δεσμού είναι γνωστή ως το μεσομερικό φαινόμενο.
Με άλλα ή πιο απλά λόγια, μπορεί να περιγραφεί ως το φαινόμενο που εμφανίζεται όταν τα pi-ηλεκτρόνια κινούνται μακριά ή προς μια ομάδα υποκαταστάτη σε ένα συζευγμένο σύστημα τροχιών. Το μεσομερικό φαινόμενο δημιουργεί συντονισμό στα μόρια. Είναι επίσης γνωστό ως ηλεκτρομερικό φαινόμενο καθώς παρέχει σταθερότητα μετατοπίζοντας ένα ζεύγος ηλεκτρονίων από το ένα μέρος στο άλλο.
Υπάρχουν δύο τύποι μεσομερικών εφέ – +M και -M.
Το ηλεκτρόνιο υπάρχει μόνο σε ορθο ή παρά θέση, καθώς το meta είναι πάντα σιωπηλό ως προς τον συντονισμό ή το μεσομερικό φαινόμενο.
Σημείωση – οι ομάδες αλκυλίου για την ενεργοποίηση του δακτυλίου βενζολίου χρησιμοποιεί άλφα-Η
Ένα σύστημα διπλού δεσμού συνδέεται απευθείας με τον άνθρακα sp3.
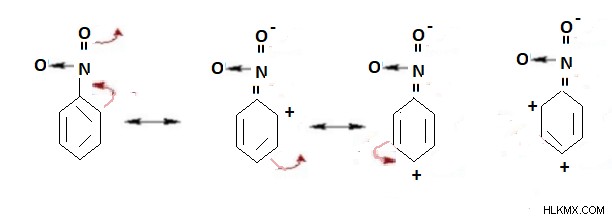
– M effect γνωστό και ως Αρνητικό μεσομερικό εφέ
Είναι η συνθήκη κατά την οποία τα ηλεκτρόνια pi λαμβάνονται από ένα συζευγμένο σύστημα και συνδέονται με μια συγκεκριμένη ομάδα .
Επομένως μειώνει την πυκνότητα ηλεκτρονίων του συζευγμένου συστήματος
Το βασικό άτομο θα έχει θετικό φορτίο
Είναι επίσης γνωστοί ως απενεργοποιητές του δακτυλίου
Οι CF3, CCl4 είναι παραδείγματα ομάδων -M
+M effect γνωστό και ως Θετικό μεσομερικό αποτέλεσμα
Είναι η κατάσταση κατά την οποία λαμβάνονται ηλεκτρόνια pi από μια συγκεκριμένη ομάδα και συνδέονται με ένα συζυγές σύστημα.
Ως εκ τούτου, αυξάνει την πυκνότητα ηλεκτρονίων στο συζευγμένο σύστημα.
Η ομάδα +M κυκλοφόρησε το αρνητικό φορτίο σε όλο τον δακτύλιο βενζολίου. 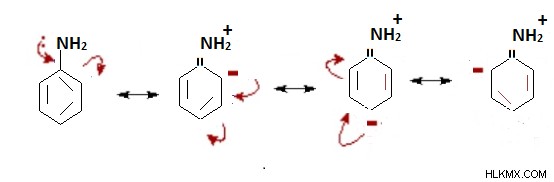
Το μεσομερικό φαινόμενο στη φαινόλη
Το μεσομερικό φαινόμενο χρησιμοποιείται για να περιγράψει χαρακτηριστικά της φαινόλης όπως οξύτητα, βασικότητα κ.λπ.
Η φαινόλη εμφανίζει θετική μεσομερική επίδραση που βοηθά στον ιονισμό της φαινόλης από ιόντα υδρογόνου και επομένως παρουσιάζει οξύτητα. Επηρεάζει επίσης το μήκος δεσμού της ένωσης.
Τα ηλεκτρόνια δεν θα υπάρχουν στη θέση Meta, δείχνοντας θετική μεσομερική επίδραση.
Οι φαινόλες είναι πιο όξινες από τις αλειφατικές αλκοόλες καθώς ο δακτύλιος βενζολίου σταθεροποιεί το ιόν του φαινοξειδίου μέσω συντονισμού μετεγκατάστασης του αρνητικού χρέωση.

Μεταγενέστερες επιδράσεις της οξύτητας των φαινολών
Οι υποκαταστάτες που δότες ηλεκτρονίων καθιστούν μια φαινόλη λιγότερο όξινη αποσταθεροποιώντας το ιόν φαινοξειδίου λόγω μεσομερούς ή συντονισμού
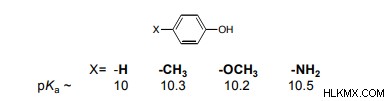
Οι υποκαταστάτες που αποσύρουν ηλεκτρονικά μέσα κάνουν τη φαινόλη πιο όξινη σταθεροποιώντας το ιόν φαινοξειδίου μέσω της μετεγκατάστασης του αρνητικού φορτίου και μέσω επαγωγικά αποτελέσματα καθώς εξουδετερώνει τα μεσομερή αποτελέσματα. 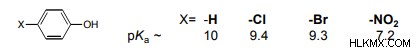
Σταθερότητα του καρβοκατιόντος φαινυλίου
Το καρβοκατιόν φαινυλίου είναι ασταθές επειδή έχει υψηλή ενέργεια θραύσης δεσμού του
δεσμός βενζολίου C-H
Επεξήγηση
Οι δεσμοί C-H των δακτυλίων βενζολίου είναι υβριδισμένοι sp2
Αυτό σημαίνει ότι υπάρχει ένας χαρακτήρας υψηλού s στον δακτύλιο λόγω του οποίου τα ηλεκτρόνια βρίσκονται πιο κοντά στο πυρήνα, που κάνει τους δεσμούς πιο δύσκολο να σπάσουν.
Προφανώς, το sp2 έχει ένα κενό τροχιακό που βρίσκεται στην επίπεδη περιοχή του δεδομένου δακτυλίου βενζολίου, το οποίο δεν μπορεί να σταθεροποιηθεί από το μεσομερικό φαινόμενο καθώς οι δεσμοί pi δεν μπορούν να το επικαλύπτουν.
Συμπέρασμα
Το μεσομερικό αποτέλεσμα θέτει τα βασικά της οξύτητας και της βασικότητας στις φαινόλες. Τα θετικά και αρνητικά μεσομερικά αποτελέσματα εξαρτώνται εξ ολοκλήρου και αποκλειστικά από τις συνδεδεμένες ομάδες και το συζευγμένο σύστημα. Ο συντονισμός μεταβάλλει το μήκος του δεσμού του δακτυλίου βενζολίου, καθιστώντας τον πιο σταθερό.
Μόνο οι θέσεις ορθο και παρά εμπλέκονται στο μεσομερικό φαινόμενο. Το μεσομερικό φαινόμενο, ειδικά το θετικό μεσομερικό φαινόμενο, υπερισχύει πάντα του αρνητικού επαγωγικού αποτελέσματος. Η μετα-θέση παραμένει πάντα αθόρυβη στο μεσομερικό φαινόμενο. Το ιόν φαινοξειδίου είναι πιο σταθερό από τη φαινόλη καθώς το μεσομερικό αποτέλεσμα λειτουργεί στη σταθερότητα του καρβοκατιόντος.
Παρόλα αυτά, το καρβοκατιόν φαινυλίου είναι αρκετά ασταθές καθώς ο συντονισμός δεν λειτουργεί εκεί, καθώς το κενό υπάρχει στο το επίπεδο sp2 και οι δεσμοί pi δεν μπορούν να το επικαλύπτουν. Όσο υψηλότερος ο συντονισμός, υψηλότερη είναι η σταθερότητα