Περιορισμένη Υδρόλυση
Η υδρόλυση περιγράφεται ως η αντίδραση μιας οργανικής ένωσης με νερό για τη δημιουργία δύο ή περισσότερων νέων ουσιών. Αναφέρεται στο σπάσιμο των χημικών δεσμών με την προσθήκη νερού. Στη χημεία, η όξινη υδρόλυση είναι μια κρίσιμη έννοια. Η φράση αναφέρεται σε μια διαδικασία στην οποία το νερό είναι το πυρηνόφιλο, όπως η εξάλειψη, η αντικατάσταση και η διαλυτοποίηση. Η βιολογική υδρόλυση είναι ένας τύπος διάσπασης βιομορίου όπου ένα μόριο νερού χρησιμοποιείται για τη διάσπαση ενός μεγαλύτερου μορίου σε μικρότερα θραύσματα. Αυτή η εργασία μιλά για το περιεχόμενο της υδρόλυσης, τη σημασία της υδρόλυσης, την έννοια της περιορισμένης υδρόλυσης και τα είδη της υδρόλυσης. Λοιπόν, χωρίς άλλη καθυστέρηση, ας ξεκινήσουμε!
Υδρόλυση στη Χημεία
Στη χημεία, η υδρόλυση είναι μια χημική αντίδραση που περιλαμβάνει όταν οι ενώσεις αλληλεπιδρούν με το νερό, με αποτέλεσμα την αποικοδόμηση τόσο του υλικού όσο και του νερού. Οι αντιδράσεις υδρόλυσης μπορούν να συμβούν με άλατα, υδατάνθρακες, πρωτεΐνες, λιπίδια και άλλες ουσίες. Η υδρόλυση μπορεί να θεωρηθεί ως το αντίστροφο μιας αντίδρασης συμπύκνωσης, στην οποία δύο μόρια συνδυάζονται για να σχηματίσουν ένα μεγαλύτερο, εκτοξεύοντας ένα μόριο νερού.
Έτσι, η υδρόλυση παρέχει το νερό για διάσπαση, ενώ η συμπύκνωση εξαλείφει τη συσσώρευση νερού. Η ενυδάτωση είναι μια επιλογή διαδικασίας κατά την οποία το νερό ενώνεται με ένα μόριο χωρίς να το αποσυντίθεται. Αυτές οι τεχνικές παράγουν αιθανόλη, γλυκόλες όπως προπυλενογλυκόλη και αιθυλενογλυκόλη και προπυλενοξείδιο.
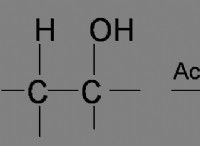
Η αλληλεπίδραση του νερού με έναν «εστέρα ενός καρβοξυλικού οξέος» μπορεί να χρησιμοποιηθεί για να δείξει υδρόλυση που περιλαμβάνει οργανικά μόρια. Όλοι αυτοί οι εστέρες έχουν τον γενικό τύπο RCO-OR', όπου οι R και R' ενώνουν ομάδες. Η δημιουργία ενός ομοιοπολικού δεσμού μεταξύ του «ατόμου οξυγόνου του μορίου του νερού και του ατόμου άνθρακα του εστέρα» είναι το πιο αργό στάδιο στη διαδικασία της υδρόλυσης. Ο σύνδεσμος άνθρακα-οξυγόνου του εστέρα διακόπτεται στα επόμενα βήματα και ιόντα υδρογόνου απελευθερώνονται από το μητρικό μόριο νερού και ενώνονται με το νεογέννητο μόριο αλκοόλης.
Τι είναι η περιορισμένη υδρόλυση;
Όταν τα ανιόντα ή τα κατιόντα δεν είναι τόσο ισχυρά όσο τα συζευγμένα τους ζεύγη, λαμβάνει χώρα υδρόλυση που σχετίζεται με την ισχύ και το υγρό μπορεί να είναι όξινο ή βασικό.
Χρήσεις περιορισμένης υδρόλυσης
Η πρώτη εμπορική χρήση της υδρόλυσης ήταν στην παραγωγή σαπουνιού. Όταν ένα τριγλυκερίδιο (γνωστό ως λίπος) υδρολύεται με νερό και μια βάση, συνήθως NaOH, υδροξείδιο του καλίου, υδροξείδιο του νατρίου ή ΚΟΗ, εμφανίζεται η αντίδραση σαπωνοποίησης. Η γλυκερόλη και τα άλατα σχηματίζονται όταν τα λιπαρά οξέα ενώνονται με τη βάση, η οποία γίνεται σαπούνι.
Μερικά παραδείγματα και χρήση της υδρόλυσης στη χημεία είναι
Ζάχαρη:Σκαρφοποίηση ονομάζεται η υδρόλυση της ζάχαρης. Για το συγκεκριμένο, η σακχαρόζη θα μπορούσε να υδρολυθεί για να απελευθερώσει την κεντρική της γλυκόζη, τα σάκχαρα και τη φρουκτόζη.
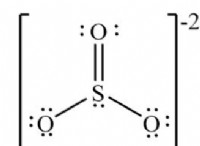
Αλάτι:Μια αντίδραση υδρόλυσης είναι η διάλυση άλατος ήπιου οξέος και βάσης στο νερό. Ισχυρά οξέα μπορούν επίσης να υδρολυθούν. Όταν το θειικό οξύ διαλύεται στο νερό, παράγει όξινο θειικό άλας και υδρόνιο.
Καταλυόμενη υδρόλυση:Η υδρόλυση τυπικά καταλύεται από ένζυμα σε βιολογικά συστήματα. Η υδρόλυση της κυτταρικής ενέργειας τριφωσφορικής αδενοσίνης, ή ATP, είναι ένα καλό παράδειγμα. Η καταλυόμενη υδρόλυση χρησιμοποιείται επίσης για την πέψη υδατανθράκων, πρωτεϊνών και λίπους.
Οξύ-βάση:Μια άλλη μορφή αντίδρασης υδρόλυσης είναι η υδρόλυση που καταλύεται με βάση οξέος.
Αλογονίδια υδρογόνου
Τα αλογονίδια του υδρογόνου είναι αέρια που αντιπροσωπεύονται από ΗΧ. Διασπώνται παρουσία νερού για να σχηματίσουν υδραλογονικά οξέα. Σε θερμοκρασία δωματίου, τα υδραλογονίδια δεν έχουν χρώμα.
Το υδροφθόριο έχει υψηλό σημείο βρασμού 20°C για μοριακά μεγέθη και μπορεί να συμπυκνωθεί όταν κρυώσει. Αυτό συμβαίνει επειδή το υδροφθόριο μπορεί να δημιουργήσει δεσμούς υδρογόνου.
Ο δεσμός φθορίου-υδρογόνου είναι πολύ πολωμένος αφού το φθόριο είναι ηλεκτραρνητικό. Το άτομο υδρογόνου έχει σημαντικό μερικό θετικό φορτίο, ενώ το άτομο φθορίου είναι αρνητικά φορτισμένο.
Ωστόσο, άλλα υδραλογονίδια δεν σχηματίζουν δεσμούς υδρογόνου επειδή τα μεγαλύτερα αλογόνα δεν είναι σχετικά ηλεκτραρνητικά. Επομένως, έχουν λιγότερους πολικούς δεσμούς. Επιπλέον, καθώς τα μόνα ζεύγη άλλων αλογόνων υπάρχουν σε υψηλότερα επίπεδα ενέργειας, τους λείπει ένα συγκεντρωμένο αρνητικό φορτίο.
Τύποι υδρόλυσης
Κάθε φορά που ένα άλας ενός όξινου διαλύματος ή μιας ασθενούς βάσης αναμιγνύεται με νερό, εμφανίζεται ένας τυπικός τύπος υδρόλυσης. Το νερό ιονίζεται αυθόρμητα σε ανιόντα υδροξειδίου και κατιόντα υδρονίου. Το αλάτι επίσης διασπάται στα συστατικά του ανιόντα και κατιόντα. Η υδρόλυση αμιδίων ή εστέρων είναι ένα παράδειγμα υδρόλυσης που καταλύεται με βάση οξέος.
Η υδρόλυση τους συμβαίνει όταν ένα πυρηνόφιλο χτυπά τον άνθρακα της καρβονυλικής ομάδας του εστέρα ή του αμιδίου. Η υδρόλυση έχει να κάνει με τις μεταβολικές δραστηριότητες και την αποθήκευση. Όλα τα ζωντανά κύτταρα απαιτούν σταθερή παροχή ενέργειας για δύο κύριες λειτουργίες:παραγωγή μικρομορίων και μακρομορίων και μεταφορά θρεπτικών ουσιών ιοντικών ειδών μέσω των κυτταρικών μεμβρανών.
Συμπέρασμα
Τα ιοντικά συστατικά του άλατος διαχωρίζονται σε διάλυμα. τα μόρια του νερού αλληλεπιδρούν με τα οξικά ιόντα για να δημιουργήσουν ιόντα υδροξειδίου και οξικό οξύ. Τα άλλα υδραλογονίδια δεν σχηματίζουν δεσμούς υδρογόνου. Οι χημικές αλλαγές που συμβαίνουν σε ένα υδατικό διάλυμα του άλατος-οξικού νατρίου μπορούν να χρησιμοποιηθούν για την απεικόνιση της υδρόλυσης ιοντικής ένωσης.
Σε διάλυμα, τα ιοντικά συστατικά του άλατος διαχωρίζονται. τα μόρια του νερού αναμιγνύονται με τα οξικά ιόντα για να παράγουν ιόντα υδροξειδίου και οξικό οξύ. Επιπλέον, τα μοναχικά τους ζευγάρια έχουν πιο σημαντικά επίπεδα ενέργειας. Δεδομένου ότι τα μοναχικά ζεύγη είναι πιο εμφανή, δεν έχουν τόση συγκέντρωση αρνητικά φορτισμένη για να προσελκύσει ποτέ το υδρογόνο.