Προσέγγιση Kossel Lewis
Ο G.N Lewis ήταν ένας διάσημος Αμερικανός χημικός που εισήγαγε την έννοια των ΣΥΜΒΟΛΩΝ LEWIS για να αναπαραστήσει το ηλεκτρόνιο σθένους σε ένα άτομο. Η θεωρία του Lewis and Kossel» μελέτησε την ηλεκτρονική διαμόρφωση των ευγενών αερίων και βρήκε το γεγονός ότι η αδράνεια των ευγενών αερίων οφείλεται στην πλήρη οκτάδα ή διπλό τους στο Ήλιο που φαίνεται να έχει δύο ηλεκτρόνια στο τελευταίο του φλοιό και προσφέρει τη γενίκευση που σημαίνει» τα άτομα που αφορούν τα διαφορετικά στοιχεία φαίνεται να συνδυάζονται για να ολοκληρώσουν τις δυάδες ή την οκτάδα τους και να επωφεληθούν από τη σταθερή ηλεκτρονική διαμόρφωση. Σε αυτό το άρθρο, θα μάθουμε για τη σημασία της θεωρίας Kossel Lewis στον σχηματισμό χημικών δεσμών.
Σημασία Συμβόλων Lewis
Ο αριθμός των κουκκίδων που περιβάλλουν το σύμβολο θα δείξει τον αριθμό των διαθέσιμων ηλεκτρονίων σθένους, κάτι που βοηθά στον υπολογισμό του τυπικού ή του ομαδικού σθένους του συγκεκριμένου στοιχείου. Σύμφωνα με την έννοια της προσέγγισης Kossel-Lewis, το άτομο που σχετίζεται με διαφορετικά στοιχεία συμμετείχε ενεργά σε συνδυασμό για να συμπληρώσει την οκτάδα τους (8 ηλεκτρόνια στο εξωτερικό κέλυφος σθένους) ή το διπλό (2 ηλεκτρόνια σθένους στο εξωτερικό κέλυφος σθένους) για την επίτευξη του πλησιέστερη διαμόρφωση ευγενούς αερίου. Αυτή η πλήρης διαδικασία είναι γνωστή ως ΚΑΝΟΝΑΣ OCTET.
Ιωνικός δεσμός:
Ένας ιοντικός δεσμός δημιουργείται από τη συνολική μεταφορά του συγκεκριμένου αριθμού ηλεκτρονίων από ένα άτομο σε άλλο άτομο για να διασφαλιστεί ότι και τα δύο θα επιτύχουν μια σταθερή ηλεκτρονική διαμόρφωση. Τα στοιχεία των ομάδων 1 και 2 σε συνδυασμό με αλογόνο, θείο και οξυγόνο δημιουργούν συνήθως ιοντικούς δεσμούς.
Υπάρχουν ορισμένες προϋποθέσεις που απαιτούνται για το σχηματισμό του ιοντικού δεσμού και παρατίθενται παρακάτω:
1. Τα άτομα που σχηματίζουν τα (κατιόντα) ιόντα, δηλαδή τα θετικά ιόντα, χρειάζονται χαμηλότερη ενέργεια ιονισμού, χαμηλή συγγένεια ηλεκτρονίων, χαμηλή ηλεκτραρνητικότητα και υψηλή ενέργεια πλέγματος.
2. Τα άτομα που σχηματίζουν ιόντα (An), δηλαδή αρνητικά ιόντα, πρέπει να έχουν υψηλή συγγένεια ηλεκτρονίων, υψηλή ηλεκτραρνητικότητα, υψηλή ενέργεια ιονισμού και ενέργεια πλέγματος.
Μερικά από τα χαρακτηριστικά των ιοντικών δεσμών ή των ηλεκτροσθενών δεσμών είναι:
Σχηματίζεται ένας ιονικός δεσμός λόγω της κουλομβικής έλξης μεταξύ των αρνητικά και θετικά φορτισμένων ιόντων.
Ένας ιοντικός δεσμός είναι μη κατευθυντικός, πράγμα που σημαίνει ότι η ισχύς της αλληλεπίδρασης μεταξύ των δύο ιόντων θα εξαρτηθεί από τον παράγοντα απόστασης και όχι από τον παράγοντα κατεύθυνσης. Ο ιονικός δεσμός σπάει όταν η ουσία διαλύεται στον πολικό διαλύτη ή όταν έχει λιώσει.
Ομοιοπολικός δεσμός
Ο ομοιοπολικός δεσμός όταν τα άτομα των ίδιων ή διαφορετικών στοιχείων θα συνδυαστούν αμοιβαία μοιράζοντας τα ηλεκτρόνια. Επομένως, μπορεί να ειπωθεί ότι ένας Ομοιοπολικός Δεσμός σχηματίζεται από την αμοιβαία κατανομή των ηλεκτρονίων, όπως ο σχηματισμός μορίων O2.
Απαιτήσεις για το σχηματισμό ομοιοπολικών δεσμών
Ορισμένες από τις απαραίτητες προϋποθέσεις για τις μορφές ομοιοπολικών δεσμών αναλύονται παρακάτω.
· Η διαφορά στην ηλεκτραρνητικότητα των μη μετάλλων δεν πρέπει να είναι υψηλή.
· Ο απλός δεσμός σημαίνει 2 ηλεκτρόνια και ακολουθούν τον κανόνα της οκτάδας μέσω της κοινής χρήσης ηλεκτρονίων. Αυτός ο τύπος μορίου φαίνεται να έχει καθορισμένο σχήμα.
Πολικός ομοιοπολικός δεσμός
Η μορφή πολικού ομοιοπολικού δεσμού ορίζεται ως ο δεσμός στον οποίο τα ηλεκτρόνια μοιράζονται μεταξύ των στοιχείων που έχουν διαφορά ηλεκτραρνητικότητας μεταξύ 0,5 και 2,0.
Διπολική στιγμή
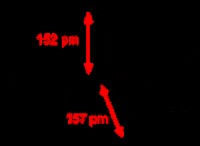
Η έννοια της διπολικής ροπής μπορεί να οριστεί ως το αποτέλεσμα του μεγέθους του φορτίου σε οποιοδήποτε από τα άτομα μαζί με την απόσταση μεταξύ τους. Έχει αναπαρασταθεί με το ελληνικό γράμμα «µ» και έχει εκφραστεί μαθηματικά, ως:
µ =e × d
Όταν το e αναφέρεται σε φορτίο σε οποιοδήποτε από τα άτομα, το d καθορίζει την απόσταση μεταξύ των ατόμων. Η μονάδα διπολικού συστήματος στο σύστημα CGS είναι το debye (D).
Τυπική χρέωση
Το επίσημο φορτίο είναι γνωστό ως το υποθετικό φορτίο που λαμβάνεται από τη δομή κουκίδων, που σημαίνει ότι είναι η διαφορά ηλεκτρικού φορτίου μεταξύ των ηλεκτρονίων σθένους στο απομονωμένο άτομο και του αριθμού ηλεκτρονίων που παρέχονται σε ένα τέτοιο άτομο στο τη δομή LEWIS.
Τυπικό φορτίο =[Αριθμός ηλεκτρονίων σθένους στο άτομο] – [μη δεσμευμένα ηλεκτρόνια + αριθμός δεσμών].
Δηλώσεις της Θεωρίας Kossel-Lewis
Όλα τα άτομα επιτυγχάνουν μια σταθερή οκτάδα, όταν συνδέονται με χημικούς δεσμούς.
Παράδειγμα αξιωμάτων της θεωρίας Kossel-Lewis
Λαμβάνοντας υπόψη το σχηματισμό NaCl, NaNaCl, το Na χάνει ένα ηλεκτρόνιο, το οποίο αποκτάται από το χλώριο. Χάνοντας ένα ηλεκτρόνιο, το NaNa θα επιτύχει τη σταθερή διαμόρφωση του Νέον, ενώ το ClCl, όταν αποκτήσει ένα ηλεκτρόνιο θα αποκτήσει τη σταθερή διαμόρφωση του αργού.
Na → Na++1e–
[Ne]3s1 [Ne]
Cl+1e– → Cl1–
[Ne]+3s23p5 [Ar]
Σημασία των θέσεων του Kossel
Τα αξιώματα του Kossel βοήθησαν σε:
Αναγνώριση και συστηματοποίηση ιοντικών ενώσεων.
Δημιουργία της βάσης για τις τελευταίες ιδέες σχηματισμού ιόντων με μεταφορά ηλεκτρονίων
Το Kossel έχει επίσης κατανοήσει το γεγονός ότι διάφορες ενώσεις δεν ταιριάζουν στις έννοιες ή τις κατηγορίες που αναφέρθηκαν. Ο Lewis έχει παράσχει τα σύμβολα για να δείξει το ηλεκτρόνιο σθένους που είναι διαθέσιμο γύρω από ένα άτομο. Ωστόσο, ο συνεργάτης του Kossel εισήγαγε το αξίωμα που εξηγούσε γιατί τα στοιχεία συνδυάζονται με το καθένα για να φτάσουν στη σταθερή ηλεκτρονική διαμόρφωση.
Συμπέρασμα
Εξηγήσαμε τη θεωρία Lewis και Kossel σχετικά με τους χημικούς δεσμούς και τη σημασία της στο σχηματισμό ιοντικών και ηλεκτροσθενών δεσμών. Η προσέγγιση Lewis-Kossel έχει μεγάλη σημασία στο σχηματισμό χημικών δεσμών.
Εάν εξακολουθείτε να έχετε αμφιβολίες ή προτάσεις, ενημερώστε μας αφήνοντας ένα σχόλιο στο παρακάτω πλαίσιο!