Διαφορά μεταξύ σύνθεσης αφυδάτωσης και υδρόλυσης
Κύρια διαφορά – Σύνθεση αφυδάτωσης έναντι υδρόλυσης
Οι χημικές αντιδράσεις μπορούν να κατηγοριοποιηθούν σε διαφορετικές ομάδες ανάλογα με τις ιδιότητες αυτών των αντιδράσεων. Η σύνθεση αφυδάτωσης και η υδρόλυση είναι τέτοιες χημικές αντιδράσεις. Αυτές οι αντιδράσεις κατηγοριοποιούνται ανάλογα με τον μηχανισμό τους. Και οι δύο αυτές αντιδράσεις περιλαμβάνουν είτε σύνθεση είτε κατανάλωση μορίων νερού. Η κύρια διαφορά μεταξύ της σύνθεσης αφυδάτωσης και της υδρόλυσης είναι ότι η σύνθεση αφυδάτωσης έχει ως αποτέλεσμα το σχηματισμό ενός μεγάλου μορίου από μικρότερα μόρια, ενώ η υδρόλυση οδηγεί στο σχηματισμό μικρότερων μορίων από ένα μεγάλο μόριο.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η σύνθεση αφυδάτωσης
– Ορισμός, Μηχανισμός, Παραδείγματα
2. Τι είναι η Υδρόλυση
– Ορισμός, Μηχανισμός, Παραδείγματα
3. Ποια είναι η διαφορά μεταξύ της σύνθεσης αφυδάτωσης και της υδρόλυσης
– Σύγκριση βασικών διαφορών
Βασικοί όροι:καρβοξυλικό οξύ, συμπύκνωση, σύνθεση αφυδάτωσης, εστεροποίηση, γλυκοσιδικός δεσμός, υδρόλυση, δεσμός πεπτιδίου

Τι είναι η Dehydration Synthesis
Η σύνθεση αφυδάτωσης είναι ο σχηματισμός ενός μεγαλύτερου μορίου με την απελευθέρωση μορίων νερού. Εδώ, δύο ή περισσότερα μικρότερα μόρια σχηματίζουν ομοιοπολικούς δεσμούς μεταξύ τους, απελευθερώνοντας ένα μόριο νερού ανά κάθε δεσμό. Επομένως, τα τελικά προϊόντα των αντιδράσεων σύνθεσης αφυδάτωσης είναι πάντα σύνθετες ενώσεις από εκείνες των αντιδρώντων. Η αντίδραση σύνθεσης αφυδάτωσης είναι ένας τύπος αντίδρασης σύνθεσης αφού παράγεται ένα μεγάλο μόριο.
Αυτές οι αντιδράσεις σύνθεσης αφυδάτωσης μπορούν επίσης να ονομαστούν αντιδράσεις συμπύκνωσης, καθώς η συμπύκνωση αναφέρεται στο σχηματισμό μορίων νερού. Επομένως, λαμβάνει χώρα σύνθεση αφυδάτωσης μεταξύ μορίων που έχουν μια ομάδα υδροξυλίου (–ΟΗ) και ενός πρωτονίου που είναι διαθέσιμα για απελευθέρωση.
Στις διαδικασίες χημικής σύνθεσης, η σύνθεση αφυδάτωσης χρησιμοποιείται για τη λήψη μεγαλύτερων μορίων μέσω της απελευθέρωσης μορίων νερού. Για παράδειγμα, η αντίδραση μεταξύ μιας αλκοόλης και ενός καρβοξυλικού οξέος μπορεί να παράγει έναν εστέρα, απελευθερώνοντας ένα μόριο νερού ως υποπροϊόν. Εδώ, απελευθερώνεται η ομάδα –ΟΗ του καρβοξυλικού οξέος και απελευθερώνεται επίσης το άτομο –Η που συνδέεται με το οξυγόνο της αλκοόλης. Επομένως, αυτές οι δύο ομάδες –ΟΗ και –Η συνδυάζονται για να σχηματίσουν ένα μόριο νερού.
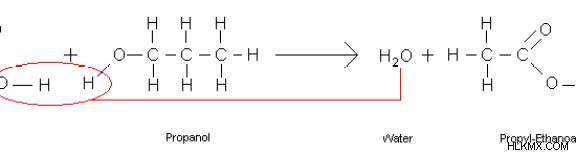
Εικόνα 01:Εστεροποίηση
Στα βιολογικά συστήματα, οι όροι γλυκοσιδικοί δεσμοί και πεπτιδικοί δεσμοί χρησιμοποιούνται συχνά για να περιγράψουν τους δεσμούς μεταξύ των μορίων. Οι γλυκοσιδικοί δεσμοί σχηματίζονται ως αποτέλεσμα της αντίδρασης μεταξύ δύο μονοσακχαριτών που απελευθερώνουν ένα μόριο νερού ενώ οι πεπτιδικοί δεσμοί σχηματίζονται ως αποτέλεσμα της αντίδρασης μεταξύ δύο αμινοξέων που απελευθερώνουν ένα μόριο νερού. Επομένως, πρόκειται για αντιδράσεις σύνθεσης συμπύκνωσης ή αφυδάτωσης.
Τι είναι η Υδρόλυση
Η υδρόλυση είναι η διάσπαση ενός χημικού δεσμού παρουσία νερού. Εδώ, το νερό λειτουργεί ως αντιδρών που εμπλέκεται στη διαδικασία της αντίδρασης. Στις αντιδράσεις υδρόλυσης, ένα μεγάλο μόριο διασπάται πάντα σε μικρότερα μόρια. Επομένως, τα αντιδρώντα περιέχουν πάντα ένα πολύπλοκο μόριο, σε αντίθεση με τα προϊόντα. Σε αυτές τις αντιδράσεις, ένα μόριο νερού προστίθεται στο μόριο του αντιδρώντος, το οποίο προκαλεί τη διάσπαση ενός χημικού δεσμού που υπάρχει σε αυτό το αντιδρών.
Όταν ένα μεγάλο μόριο υδρολύεται, τα δύο μικρά μόρια που προκύπτουν παίρνουν μια ομάδα –ΟΗ και μια ομάδα –Η από το μόριο του νερού. Η υδρόλυση είναι το αντίθετο της συμπύκνωσης. Αυτό συμβαίνει επειδή, στις αντιδράσεις συμπύκνωσης, σχηματίζεται ένα μόριο νερού ενώ στην υδρόλυση καταναλώνεται ένα μόριο νερού.
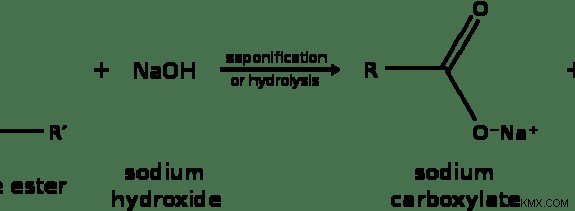
Εικόνα 2:Αντίδραση υδρόλυσης εστέρα
Αν πάρουμε το ίδιο παράδειγμα όπως στην αντίδραση σύνθεσης αφυδάτωσης, η υδρόλυση ενός εστέρα σχηματίζει τα αντιδρώντα της αντίδρασης εστεροποίησης. Είναι το καρβοξυλικό οξύ και το αλκοόλ. Για αυτό, χρησιμοποιείται μια βάση. Ως εκ τούτου, σχηματίζεται καρβοξυλικό ιόν αντί για καρβοξυλικό οξύ λόγω της υψηλής σταθερότητάς του. Ωστόσο, αυτή η αντίδραση καταναλώνει μόρια νερού για να δώσει την ομάδα –ΟΗ για το σχηματισμό καρβοξυλικού οξέος και την ομάδα –Η για το σχηματισμό αλκοόλης. Αυτή η διαδικασία ονομάζεται σαπωνοποίηση.
Διαφορά μεταξύ σύνθεσης αφυδάτωσης και υδρόλυσης
Ορισμός
Αφυδάτωση: Η σύνθεση αφυδάτωσης είναι ο σχηματισμός ενός μεγαλύτερου μορίου με την απελευθέρωση μορίων νερού.
Υδρόλυση: Η υδρόλυση είναι η διάσπαση ενός χημικού δεσμού παρουσία νερού.
Μηχανισμός
Αφυδάτωση: Οι αντιδράσεις σύνθεσης αφυδάτωσης είναι αντιδράσεις συνδυασμού.
Υδρόλυση: Οι αντιδράσεις υδρόλυσης είναι αντιδράσεις αποσύνθεσης.
Μόριο νερού
Αφυδάτωση: Η αντίδραση σύνθεσης αφυδάτωσης σχηματίζει ένα μόριο νερού.
Υδρόλυση: Η αντίδραση υδρόλυσης καταναλώνει ένα μόριο νερού.
Αντιδρώντα
Αφυδάτωση: Τα αντιδρώντα των αντιδράσεων σύνθεσης αφυδάτωσης είναι μικρότερα μόρια από τα προϊόντα τους.
Υδρόλυση: Τα αντιδρώντα των αντιδράσεων υδρόλυσης είναι πολύπλοκα μόρια από τα προϊόντα τους.
Υποπροϊόντα
Αφυδάτωση: Οι αντιδράσεις σύνθεσης αφυδάτωσης δίνουν μόρια νερού ως υποπροϊόντα.
Υδρόλυση: Οι αντιδράσεις υδρόλυσης δεν δίνουν υποπροϊόντα.
Συμπέρασμα
Τόσο η σύνθεση αφυδάτωσης όσο και η υδρόλυση είναι χημικές αντιδράσεις που συμβαίνουν παρουσία νερού. Αυτό συμβαίνει επειδή οι αντιδράσεις σύνθεσης αφυδάτωσης παρέχουν μόρια νερού στο μέσο, ενώ οι αντιδράσεις υδρόλυσης καταναλώνουν μόρια νερού από το μείγμα αντίδρασης. Η κύρια διαφορά μεταξύ της σύνθεσης αφυδάτωσης και της υδρόλυσης είναι ότι η σύνθεση αφυδάτωσης έχει ως αποτέλεσμα το σχηματισμό ενός μεγάλου μορίου από μικρότερα μόρια, ενώ η υδρόλυση οδηγεί σε μικρότερα μόρια από ένα μεγάλο μόριο.




