Διαφορά μεταξύ Στερικής και Στρεπτικής Καταπόνησης
Κύρια διαφορά – Steric vs Torsional Strain
Το στέλεχος είναι η απώθηση μεταξύ ηλεκτρονίων δεσμού ενός μορίου. Η διάταξη ενός μορίου εξαρτάται από το στέλεχος αφού τα ζεύγη ηλεκτρονίων δεσμών είναι διατεταγμένα με τρόπο που ελαχιστοποιεί την τάση. Υπάρχουν τρεις κύριοι τύποι στελεχών που μπορούν να βρεθούν σε ένα μόριο. Είναι η γωνιακή τάση, η στρεπτική τάση και η στερική τάση. Η γωνιακή τάση εμφανίζεται όταν οι γωνίες δεσμού των πραγματικών μορίων είναι διαφορετικές από αυτές των ιδανικών μορίων. Η στρεπτική τάση προκύπτει όταν ένα μόριο περιστρέφεται γύρω από έναν δεσμό. Το στερικό στέλεχος σχηματίζεται όταν δύο ή περισσότερες ογκώδεις ομάδες πλησιάζουν η μία την άλλη. Η κύρια διαφορά μεταξύ στερικής και στρεπτικής τάσης είναι ότι η στερική καταπόνηση δεν μπορεί να μειωθεί περιστρέφοντας το μόριο γύρω από έναν δεσμό, ενώ η στρεπτική τάση μπορεί να μειωθεί περιστρέφοντας το μόριο γύρω από έναν δεσμό.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το Steric Strain
– Ορισμός, εξήγηση με παραδείγματα
2. Τι είναι η στρεπτική καταπόνηση
– Ορισμός, Εξήγηση με Παραδείγματα
3. Ποια είναι η διαφορά μεταξύ Στερικής και Στρεπτικής Καταπόνησης
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Γωνιακή παραμόρφωση, Ζεύγος ηλεκτρονίων δεσμού, Στειρική παραμόρφωση, Στρεπτική παραμόρφωση
Τι είναι το Steric Strain
Η στερική τάση είναι η απώθηση μεταξύ δύο ατόμων ή ομάδων ατόμων όταν η απόσταση μεταξύ τους μειώνεται. Αυτό ονομάζεται επίσης στερική παρεμπόδιση . Το στερικό στέλεχος είναι πολύ σημαντικό για τον προσδιορισμό της διάταξης ενός μορίου αφού κάθε μόριο είναι διατεταγμένο με τέτοιο τρόπο ώστε το στερικό στέλεχος να ελαχιστοποιείται. Όταν το στερικό στέλεχος ελαχιστοποιείται, η δυναμική ενέργεια αυτού του μορίου μειώνεται. Εφόσον η ύλη είναι σταθερή όταν έχει χαμηλότερο ενεργειακό επίπεδο, το χαμηλότερο ενεργειακό επίπεδο ενός μορίου το καθιστά σταθερό μόριο.
Η έννοια του στερικού στελέχους είναι πολύ σημαντική για την πρόβλεψη των προϊόντων μιας χημικής αντίδρασης. Αυτό συμβαίνει επειδή ομάδες ατόμων συνδέονται με ένα άτομο άνθρακα με τέτοιο τρόπο ώστε να ελαχιστοποιείται το στερικό εμπόδιο. Επομένως, μια χημική αντίδραση θα δώσει ένα μείγμα μορίων όπου περιλαμβάνονται σταθερά προϊόντα και ασταθή προϊόντα. Αλλά το κύριο συστατικό αυτού του μείγματος θα είναι πάντα το σταθερό προϊόν με ελαχιστοποιημένο στερεοχημικό εμπόδιο.
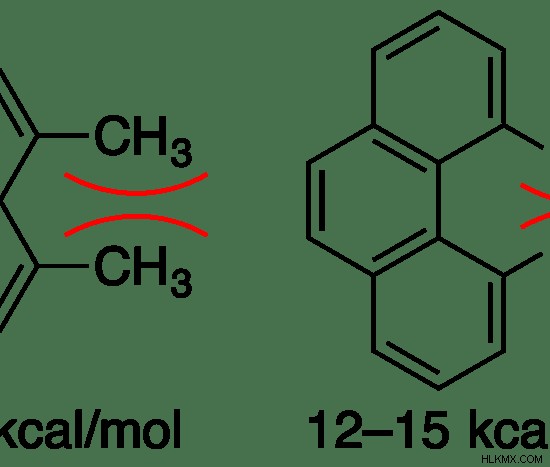
Εικόνα 1:Στερικό στέλεχος σε οργανικές ενώσεις
Όπως φαίνεται στην παραπάνω εικόνα, η δυναμική ενέργεια ενός μορίου αυξάνεται ανάλογα με τη στερική τάση που έχει. Όταν η απόσταση μεταξύ δύο ομάδων μεθυλίου μειώνεται, η δυναμική ενέργεια αυξάνεται.
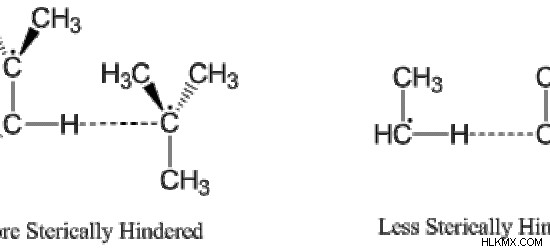
Εικόνα 2:Στερική καταπόνηση αυξάνεται όταν υπάρχουν ογκώδεις ομάδες
Η παραπάνω εικόνα δείχνει ότι η στερική καταπόνηση αυξάνεται όταν υπάρχουν ογκώδεις ομάδες. Τα πιο στερικά παρεμποδισμένα μόρια έχουν υψηλότερη δυναμική ενέργεια σε σύγκριση με τα λιγότερο στερεοχημικά παρεμποδισμένα μόρια. Επομένως, τα μόρια με λιγότερο στερεοχημική παρεμπόδιση είναι πιο σταθερά.
Τι είναι η Στρεπτική Παραμόρφωση
Η στρεπτική τάση είναι η απώθηση που προκύπτει μεταξύ ατόμων ή ομάδων ατόμων όταν ένα μόριο περιστρέφεται γύρω από έναν δεσμό σίγμα. Αυτή είναι η απώθηση που μπορεί να παρατηρηθεί όταν τα ηλεκτρόνια του δεσμού περνούν το ένα από το άλλο. Αυτός ο τύπος στελέχους είναι σημαντικός για τον προσδιορισμό των σταθερών διαμορφώσεων των οργανικών ενώσεων. Αυτές οι διαμορφώσεις μπορούν να αναπαρασταθούν με προβολές Newman. Η προβολή Newman ενός μορίου είναι η διαμόρφωση αυτού του μορίου όταν εξετάζεται μέσω του δεσμού C-C από την μπροστινή προς τα πίσω κατεύθυνση.
Η στρεπτική τάση προκύπτει όταν η διεδρική γωνία των ογκωδών ομάδων είναι χαμηλή. Η διεδρική γωνία είναι η γωνία μεταξύ δύο δεσμών δύο διαφορετικών ατόμων άνθρακα σε μια προβολή Newman. Εάν η διεδρική γωνία είναι υψηλή, τότε η στρεπτική τάση είναι χαμηλή.
Οι προβολές Newman μπορούν να βρεθούν σε δύο τύπους, όπως η κλιμακωτή διαμόρφωση και η επισκιασμένη διαμόρφωση. Η διαμόρφωση έκλειψης παρουσιάζει υψηλή στρεπτική τάση από αυτή της κλιμακωτής διαμόρφωσης.
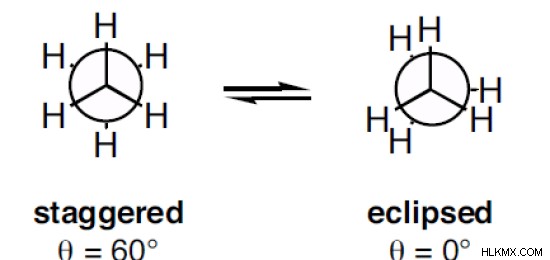
Εικόνα 3:Δύο τύποι προβολής Newman
Όπως φαίνεται στην παραπάνω εικόνα, η κλιμακωτή διαμόρφωση δείχνει μια διεδρική γωνία 60 και η επισκιασμένη διαμόρφωση δείχνει μια διεδρική γωνία 0. Αλλά όταν το μόριο περιστρέφεται, η διαμόρφωση αλλάζει. Η στρεπτική καταπόνηση σε κλιμακωτή διαμόρφωση είναι χαμηλότερη από αυτή της διαμόρφωσης έκλειψης. Όταν το μόριο περιστρέφεται, η επισκιασμένη διαμόρφωση μπορεί να γίνει η κλιμακωτή διαμόρφωση. Έτσι, η στρεπτική τάση μειώνεται.
Διαφορά μεταξύ στερικής και στρεπτικής τάσης
Ορισμός
Στειρικό στέλεχος: Το στερικό στέλεχος είναι η απώθηση μεταξύ δύο ατόμων ή ομάδων ατόμων όταν η απόσταση μεταξύ τους μειώνεται.
Στρέψη: Η στρεπτική τάση είναι η απώθηση που προκύπτει μεταξύ ατόμων ή ομάδων ατόμων όταν ένα μόριο περιστρέφεται γύρω από έναν δεσμό σίγμα.
Περιστροφή του μορίου
Στειρικό στέλεχος: Το στερικό στέλεχος δεν μπορεί να μειωθεί με την περιστροφή του μορίου γύρω από έναν δεσμό σίγμα.
Στρέψη: Η στρεπτική καταπόνηση μπορεί να μειωθεί περιστρέφοντας το μόριο γύρω από έναν δεσμό σίγμα.
Αιτία για το στέλεχος
Στειρικό στέλεχος: Η στερική καταπόνηση εμφανίζεται όταν η απόσταση μεταξύ ογκωδών ομάδων ενός μορίου μειώνεται.
Στρέψη: Η στρεπτική τάση εμφανίζεται όταν τα ηλεκτρόνια του δεσμού περνούν το ένα δίπλα στο άλλο όταν το μόριο περιστρέφεται.
Συμπέρασμα
Η καταπόνηση ενός μορίου είναι η απώθηση μεταξύ ηλεκτρονίων δεσμού ή μεμονωμένων ζευγών ηλεκτρονίων που υπάρχουν σε αυτό το μόριο. Αυτή η απώθηση προκαλεί την αύξηση της δυναμικής ενέργειας ενός μορίου. Στη συνέχεια, κάνει το μόριο ασταθές. Το στερικό στέλεχος ενός μορίου προσδιορίζεται από τις ογκώδεις ομάδες που υπάρχουν σε ένα μόριο και την απόσταση μεταξύ αυτών των ογκωδών ομάδων. Η προβολή Newman είναι μια απλή δομή που δείχνει τη διάταξη ατόμων ή ομάδων ατόμων σε ένα οργανικό μόριο. Μπορεί να χρησιμοποιηθεί για τον προσδιορισμό της στρεπτικής τάσης ενός μορίου. Η κύρια διαφορά μεταξύ της στερικής και της στρεπτικής τάσης είναι ότι η στερική τάση δεν μπορεί να μειωθεί περιστρέφοντας το μόριο γύρω από έναν δεσμό, ενώ η στρεπτική τάση μπορεί να μειωθεί περιστρέφοντας το μόριο γύρω από έναν δεσμό.