Διαφορά μεταξύ τυποποίησης και ογκομέτρησης
Κύρια διαφορά – Τυποποίηση έναντι ογκομέτρησης
Η τυποποίηση και η τιτλοποίηση είναι δύο σχετικοί χημικοί όροι. Αν και χρησιμοποιούν την ίδια τεχνική για να πάρουν μια μέτρηση, οι εφαρμογές τους είναι διαφορετικές μεταξύ τους. Η τυποποίηση χρησιμοποιείται για τον προσδιορισμό της ακριβούς συγκέντρωσης ενός παρασκευασμένου διαλύματος. Οι τιτλοδοτήσεις χρησιμοποιούνται για τον προσδιορισμό των άγνωστων συγκεντρώσεων των δειγμάτων. Τις περισσότερες φορές, η τυποποίηση γίνεται και ως τιτλοδότηση. Η κύρια διαφορά μεταξύ τυποποίησης και τιτλοδότησης είναι ότι οι διεργασίες τυποποίησης χρησιμοποιούν ουσιαστικά πρωτεύοντα πρότυπα διαλύματα ενώ οι τιτλοδοτήσεις δεν χρησιμοποιούν ουσιαστικά πρωτεύοντα πρότυπα διαλύματα.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η Τυποποίηση
– Ορισμός, Τεχνική
2. Τι είναι η ογκομέτρηση
– Ορισμός, Τεχνική
3. Ποια είναι η διαφορά μεταξύ τυποποίησης και ογκομέτρησης
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Τελικό σημείο, σημείο ισοδυναμίας, δείκτης, πρωτεύον πρότυπο, δευτερεύον πρότυπο, τυποποίηση, τιτλοδότηση

Τι είναι η Τυποποίηση
Η τυποποίηση είναι η τεχνική που χρησιμοποιείται για την εύρεση της ακριβούς συγκέντρωσης μιας λύσης. Η πιο συχνά χρησιμοποιούμενη τεχνική για την τυποποίηση ενός διαλύματος είναι η τιτλοδότηση. Για μια διαδικασία τυποποίησης, απαιτείται μια τυπική λύση ως αναφορά. Τα τυπικά διαλύματα μπορούν να βρεθούν σε δύο τύπους ως πρωτογενή τυπικά διαλύματα και δευτερεύοντα πρότυπα διαλύματα. Για ακριβείς τυποποιήσεις, χρησιμοποιούμε πρωτογενείς τυπικές λύσεις. Αυτά τα διαλύματα έχουν υψηλή καθαρότητα.

Εικόνα 1:Η σκόνη καθαρού σιδήρου είναι ένα κύριο πρότυπο
Όταν φτιάχνουμε ένα διάλυμα χρησιμοποιώντας μια στερεά χημική ένωση, η τελική συγκέντρωση αυτού του διαλύματος μπορεί να ποικίλλει ανάλογα με διάφορους παράγοντες όπως η καθαρότητα της ένωσης, τα σφάλματα οργάνων, τα ανθρώπινα λάθη κ.λπ. Για παράδειγμα, αν θέλουμε να φτιάξουμε ένα διάλυμα EDTA 1,0 mol, μπορούμε να ζυγίσουμε την κατάλληλη ποσότητα που απαιτείται για την παρασκευή και να τη διαλύσουμε σε κατάλληλο όγκο νερού. Το απαιτούμενο βάρος μπορεί να υπολογιστεί χρησιμοποιώντας τα δεδομένα που αναγράφονται στην ετικέτα της φιάλης. Αλλά αυτό μπορεί να μην δώσει την ακριβή συγκέντρωση που χρειαζόμαστε. Επομένως, μετά την παρασκευή του διαλύματος, θα πρέπει να τυποποιηθεί χρησιμοποιώντας ένα πρωτεύον πρότυπο διάλυμα για να βρεθεί η ακριβής συγκέντρωση του παρασκευασμένου διαλύματος.
Τι είναι η τιτλοδότηση
Η τιτλοδότηση είναι μια χημική τεχνική που χρησιμοποιείται για τη μέτρηση της συγκέντρωσης ενός συγκεκριμένου χημικού συστατικού σε ένα δεδομένο διάλυμα. Αυτό γίνεται χρησιμοποιώντας ένα διάλυμα που έχει γνωστή συγκέντρωση. Μια τιτλοδότηση γίνεται με τη χρήση μιας συγκεκριμένης συσκευής. Αυτή η συσκευή δίνεται στην παρακάτω εικόνα.
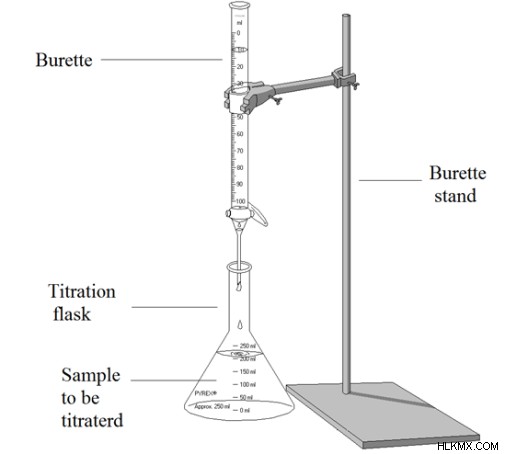
Εικόνα 2:Συσκευή ογκομέτρησης
Η προχοΐδα είναι γενικά γεμάτη με ένα πρότυπο διάλυμα με γνωστή συγκέντρωση. Εάν όχι, το διάλυμα στην προχοΐδα θα πρέπει να τυποποιηθεί χρησιμοποιώντας ένα πρωτεύον πρότυπο. Η φιάλη τιτλοδότησης γεμίζεται με το δείγμα που έχει το χημικό συστατικό με άγνωστη συγκέντρωση. Εάν το τυποποιημένο διάλυμα (σε προχοΐδα) δεν μπορεί να λειτουργήσει ως αυτοδείκτης, θα πρέπει να προσθέσουμε έναν κατάλληλο δείκτη στο δείγμα στη φιάλη τιτλοδότησης. Στη συνέχεια, το τυποποιημένο διάλυμα προστίθεται αργά στη φιάλη μέχρι να παρατηρηθεί αλλαγή χρώματος. Η αλλαγή χρώματος στη φιάλη τιτλοδότησης υποδεικνύει το τελικό σημείο της ογκομέτρησης. Αν και δεν είναι το ακριβές σημείο στο οποίο τελειώνει η ογκομέτρηση, μπορούμε να το λάβουμε ως ισοδύναμο σημείο, καθώς υπάρχει μόνο μια μικρή διαφορά.
Η ανάγνωση της προχοΐδας μπορεί να χρησιμοποιηθεί για να βρεθεί η ποσότητα του τυπικού διαλύματος που αντέδρασε με το δείγμα. Στη συνέχεια, χρησιμοποιώντας χημικές αντιδράσεις και στοιχειομετρικές σχέσεις, μπορούμε να προσδιορίσουμε τη συγκέντρωση του αγνώστου.
Διαφορά μεταξύ τυποποίησης και ογκομέτρησης
Ορισμός
Τυποποίηση: Η τυποποίηση είναι η τεχνική που χρησιμοποιείται για την εύρεση της ακριβούς συγκέντρωσης ενός διαλύματος.
Τιτλοδότηση: Η τιτλοδότηση είναι η τεχνική που χρησιμοποιείται για τη μέτρηση της συγκέντρωσης ενός συγκεκριμένου χημικού συστατικού σε ένα δεδομένο διάλυμα.
Εφαρμογή
Τυποποίηση: Η τυποποίηση χρησιμοποιείται για να βρεθεί η ακριβής συγκέντρωση ενός διαλύματος που παρασκευάζεται για άλλη ανάλυση.
Τιτλοδότηση: Η τιτλοδότηση χρησιμοποιείται για την εύρεση της άγνωστης συγκέντρωσης ενός χημικού συστατικού σε ένα δεδομένο δείγμα.
Λύση σε Burette
Τυποποίηση: Για τυποποίηση, η προχοΐδα γεμίζεται με ένα πρωτεύον πρότυπο διάλυμα.
Τιτλοδότηση: Για τιτλοδότηση, η προχοΐδα γεμίζεται είτε με πρωτεύον πρότυπο διάλυμα είτε με οποιοδήποτε άλλο τυποποιημένο διάλυμα.
Λύση σε φιάλη τιτλοδότησης
Τυποποίηση: Για τυποποίηση, το διάλυμα που πρέπει να τυποποιηθεί εισάγεται στη φιάλη τιτλοδότησης.
Τιτλοδότηση: Για τιτλοδότηση λαμβάνεται το διάλυμα που έχει το χημικό συστατικό με άγνωστη συγκέντρωση.
Συμπέρασμα
Οι τυποποιήσεις γίνονται συχνά ως τιτλοδοτήσεις λόγω της ευκολίας χειρισμού. Επομένως είναι σχετικοί χημικοί όροι. Η κύρια διαφορά μεταξύ τυποποίησης και τιτλοδότησης είναι ότι οι διαδικασίες τυποποίησης χρησιμοποιούν ουσιαστικά πρωτεύοντα πρότυπα διαλύματα, ενώ οι τιτλοδοτήσεις δεν χρησιμοποιούν ουσιαστικά πρωτεύοντα πρότυπα διαλύματα.