Τι συμβαίνει σε μια αντίδραση οξέος βάσης σύμφωνα με τον ορισμό του Arrhenius;
Όταν αντιδρούν ένα οξύ και μια βάση, τα ιόντα υδρογόνου από το οξύ και τα ιόντα υδροξειδίου από τη βάση συνδυάζονται για να σχηματίσουν νερό (H2O). Αυτή η αντίδραση είναι γνωστή ως εξουδετέρωση.
Η καθαρή ιοντική εξίσωση για μια αντίδραση εξουδετέρωσης είναι:
H + + OH- → H2O
Για παράδειγμα, όταν αντιδρούν το υδροχλωρικό οξύ (HCl) και το υδροξείδιο του νατρίου (NaOH), εμφανίζεται η ακόλουθη αντίδραση εξουδετέρωσης:
HCl + NaOH → NaCl + H2O
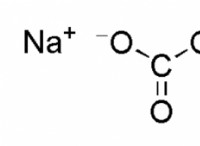
Τα προϊόντα μιας αντίδρασης εξουδετέρωσης είναι άλας και νερό. Το αλάτι αποτελείται από τα θετικά φορτισμένα ιόντα από τη βάση και τα αρνητικά φορτισμένα ιόντα από το οξύ.
Οι αντιδράσεις εξουδετέρωσης είναι σημαντικές σε πολλές καθημερινές εφαρμογές, όπως:
* Η παραγωγή αντιόξινων για την εξουδετέρωση του οξέος του στομάχου
* Η χρήση της σόδα ψησίματος για την εξουδετέρωση των οξέων στο ψήσιμο
* Η επεξεργασία του νερού για την απομάκρυνση των ακαθαρσιών
Ο ορισμός του Arrhenius των οξέων και των βάσεων είναι ένας απλός και χρήσιμος τρόπος για να κατανοήσουμε πώς αντιδρούν αυτές οι ουσίες. Ωστόσο, δεν είναι ο μόνος ορισμός των οξέων και των βάσεων. Άλλοι ορισμοί, όπως ο ορισμός του Bronsted-Lowry και ο ορισμός του Lewis, παρέχουν διαφορετικές γνώσεις στη συμπεριφορά των οξέων και των βάσεων.