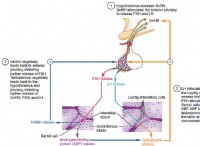
Πόσα moles CO2 σχηματίζονται όταν 58 g βουτάνιο C4H10 καίγονται σε οξυγόνο;
$$ 2C_4H_ {10} + 13O_2 -> 8CO_2 + 10H_2O $$
Πρώτον, υπολογίστε τον αριθμό των γραμμομορίων του βουτανίου σε 58 g:
$$ moles \ c_4h_ {10} =\ frac {58 g} {58.12 g/mol} =1.00 mol $$
Σύμφωνα με την ισορροπημένη χημική εξίσωση, 2 γραμμομονείς βουτανίου παράγουν 8 γραμμομονείς διοξειδίου του άνθρακα. Επομένως, 1 mole του βουτανίου θα παράγει:
$$ moles \ co_2 =1,00 mol \ c_4h_ {10} \ times \ frac {8 mol \ co_2} {2 mol \ c_4h_ {10}} $$
$$ moles \ co_2 =4.00 mol $$
Έτσι, όταν σχηματίζονται 58 g βουτανίου σε οξυγόνο, σχηματίζονται 4,00 moles διοξειδίου του άνθρακα.