Ποια ένωση απελευθερώνει ιόντα όταν βρίσκονται σε λύσεις;
Εδώ είναι μια κατανομή:
* ιόντα: Άτομα ή μόρια που έχουν κερδίσει ή χαμένα ηλεκτρόνια, δίνοντάς τους ένα θετικό ή αρνητικό φορτίο.
* Electrolytes: Ουσίες που μπορούν να διεξάγουν ηλεκτρική ενέργεια όταν διαλύονται σε νερό. Αυτή η αγωγιμότητα οφείλεται στην κίνηση των ιόντων.
Παραδείγματα ηλεκτρολυτών:
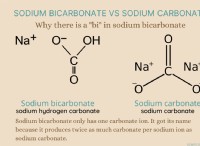
* άλατα: Όπως το επιτραπέζιο αλάτι (NaCl), το οποίο διαχωρίζεται σε ιόντα νατρίου (Na+) και χλωριούχα ιόντα (Cl-) σε νερό.
* οξέα: Όπως το υδροχλωρικό οξύ (HCl), το οποίο διαχωρίζεται σε ιόντα υδρογόνου (Η+) και σε ιόντα χλωριούχου (CL-) σε νερό.
* βάσεις: Όπως το υδροξείδιο του νατρίου (NaOH), το οποίο διαχωρίζεται σε ιόντα νατρίου (Na+) και ιόντα υδροξειδίου (ΟΗ-) στο νερό.
Μη ηλεκτρολυτικά είναι ενώσεις που δεν απελευθερώνουν ιόντα όταν διαλύονται σε διάλυμα. Αυτές οι ουσίες δεν διεξάγουν ηλεκτρική ενέργεια.
Παραδείγματα μη ηλεκτρολυτών:
* σάκχαρα: Όπως η γλυκόζη (C6H12O6)
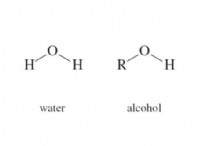
* αλκοόλες: Όπως η αιθανόλη (C2H5OH)
* Οι περισσότερες οργανικές ενώσεις: Σαν λίπη και έλαια
Επιτρέψτε μου να ξέρω αν έχετε άλλες ερωτήσεις!